Pravin U. Dugel, MD
Phoenix
/p>
Edema macular de cistoide Pseudofáquico foi primeiro descrito por A. Ray Irvine Jr., MD,1 em 1953 e mais elucidado por J. Donald M Gass, MD, em 1969.2 Dr. Gass descreveu que o pico de incidência ocorreu às seis semanas de pós-operatório, e sugeriu que havia uma diferença entre PCME angiográfico versus PCME clinicamente significativo, na medida em que apenas alguns pacientes se queixaram de visão diminuída. A PCME clínica é agora definida como uma acuidade visual de Snellen de 20/40 ou pior. Os sintomas comuns incluem diminuição da acuidade visual e sensibilidade ao contraste, bem como metamorfoses.
br> Embora a adopção da facoemulsificação sobre a remoção extracapsular da catarata tenha diminuído a taxa de PCME de 16 para 24 por cento,3 o uso crescente de implantes de lentes intraoculares multifocais levou a maiores expectativas por parte dos pacientes. Devido à concepção destes novos implantes, que inerentemente diminuem a sensibilidade ao contraste, mesmo a PCME ligeira pode resultar numa redução significativa da qualidade de visão e da satisfação dos pacientes. Quando a Food and Drug Administration aprova a utilização de qualquer nova IOL, declara que a “taxa aceitável” de PCME clinicamente significativa deve ser inferior a 5 por cento. Dada a rápida evolução da tecnologia cirúrgica e da IOL, a PCME “clinicamente significativa” pode necessitar de ser redefinida para se adaptar tanto aos requisitos visuais como às expectativas do paciente.
br>Incidência
A incidência de PCME após a facoemulsificação em pacientes não complicados e de baixo risco pode variar de 2% a 12%.4,5 Pensa-se que a incidência máxima ocorre seis semanas após a cirurgia.2 Factores preditivos do desenvolvimento da PCME nesta população incluem um historial de oclusão da veia retiniana, a presença de uma membrana epiretiniana, e o uso pré-operatório de prostaglandina.4 Em doentes com características de alto risco, como a diabetes mellitus, ou em casos complicados, a incidência pode ser muito maior. (Heier JS, et al. Características dos pacientes com EMC após a facoemulsificação. Apresentado na Reunião Anual da Academia Americana de Oftalmologia; Novembro de 2007; Nova Orleães, LA.)
br>Mecanismo
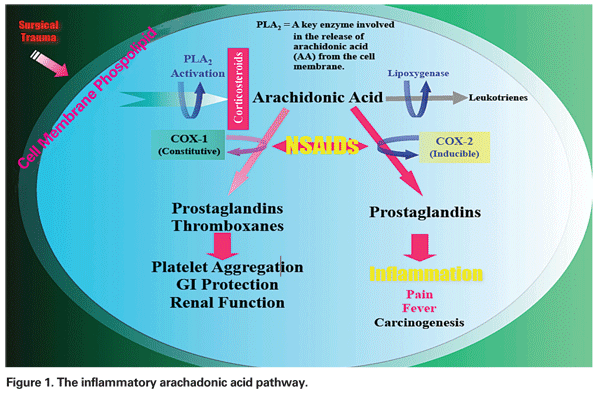
O mecanismo pelo qual a PCME se desenvolve pode ser multifactorial, tendo vários graus de componentes inflamatórios e mecânicos. A manipulação cirúrgica do segmento anterior desencadeia a libertação de ácido araquadónico das membranas celulares, o que leva à produção de prostaglandinas e leucotrienos através das vias da ciclo-oxigenase (COX) e da lipoxigenase (LOX), respectivamente (Ver Figura 1). Estes mediadores inflamatórios aumentam a vasopermeabilidade, levando assim ao desenvolvimento de PCME.
 br>>Ocasionalmente, a inflamação produzida pela extracção de cataratas pode causar contracção da face hialóide posterior, levando à distorção dos capilares parafoidais e ao consequente edema macular. O uso crescente da tomografia de coerência óptica tornou-se uma parte importante na avaliação da PCME. As imagens OCT são úteis na identificação de um componente mecânico da CME, incluindo a tracção vitreomacular ou membranas epiretinais (Ver Figuras 2 & 3).
br>>Ocasionalmente, a inflamação produzida pela extracção de cataratas pode causar contracção da face hialóide posterior, levando à distorção dos capilares parafoidais e ao consequente edema macular. O uso crescente da tomografia de coerência óptica tornou-se uma parte importante na avaliação da PCME. As imagens OCT são úteis na identificação de um componente mecânico da CME, incluindo a tracção vitreomacular ou membranas epiretinais (Ver Figuras 2 & 3).
br>> Em casos raros de PCME crónica, refractária em pacientes de baixo risco sem qualquer outra etiologia identificável, o olho deve ser escrutinado de perto para detectar fragmentos de lente retidos, malposição de IOL ou a presença de infecção por Propionibacterium acnes.
br>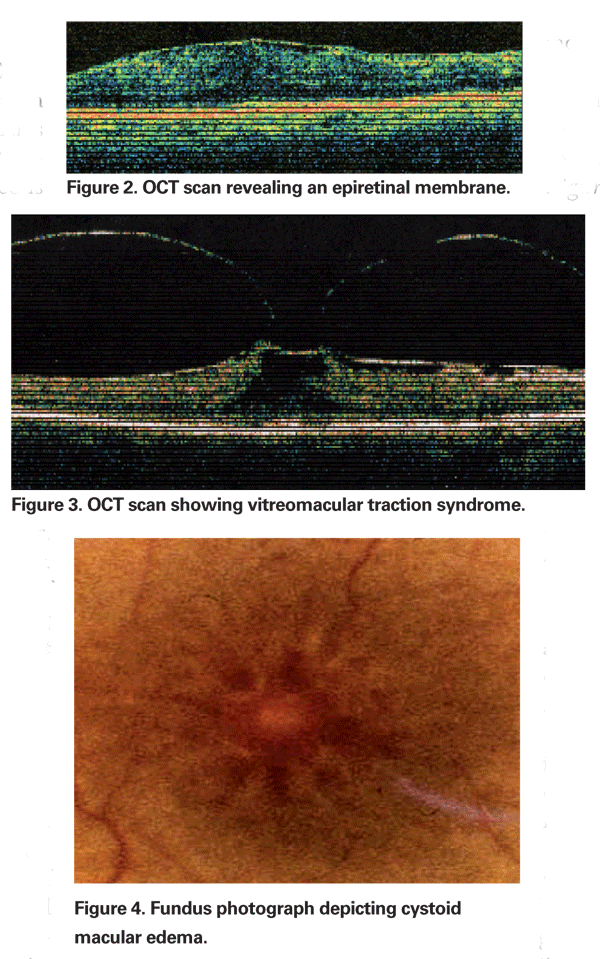
br>Diagnóstico
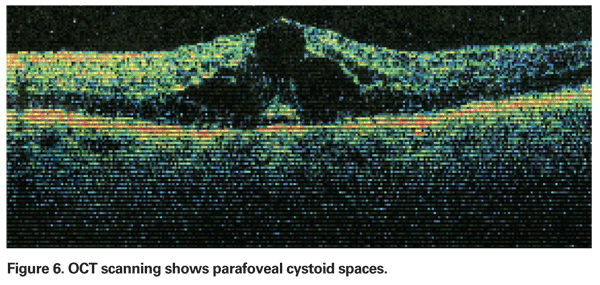
PCME deve ser suspeito quando um paciente sem factores de risco subjacentes se queixa de visão reduzida ou metamorfoses após a extracção de cataratas. Clinicamente, pode ser observado um edema intra-retinal contido em espaços semelhantes a cistos num padrão de favo de mel à volta da fovea (ver Figura 4). No angiograma de fluoresceína, pode ser observado um padrão de fuga de pétaloides para os espaços intra-retinais parafoveais, juntamente com hiperfluorescência do disco óptico (Ver figura 5). A OCT pode demonstrar claramente estes espaços cistóides, bem como calcular a espessura macular central e o volume macular total (Ver Figura 6). As vantagens da TCO são a sua alta sensibilidade, não invasividade, entrega de informação anatómica, e capacidade de quantificar o edema macular, embora haja uma correlação questionável entre estes valores e a função visual.
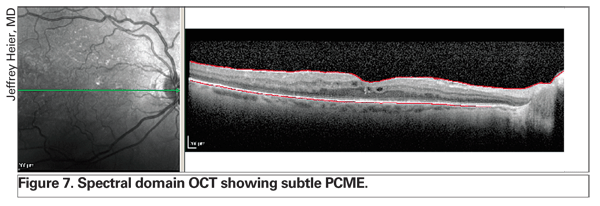
br> O uso de OCT está a revolucionar a gestão do edema da retina. A tecnologia mais recente, incluindo OCT de domínio espectral, proporciona melhor resolução e pode detectar a PCME subtil mais cedo do que a biomicroscopia com lâmpada de fenda e a angiografia com fluoresceína (Ver Figura 7). Além disso, esta instrumentação melhorada permite ao clínico distinguir entre edema exclusivamente intraretinal e fluido epitelial subretinal ou subpigmentar, o que pode fornecer informação prognóstica (Ver Figura 8). Tem sido a experiência de vários especialistas em retina que a presença de um descolamento epitelial de um pigmento subfoveal pode representar um pior prognóstico.
>br>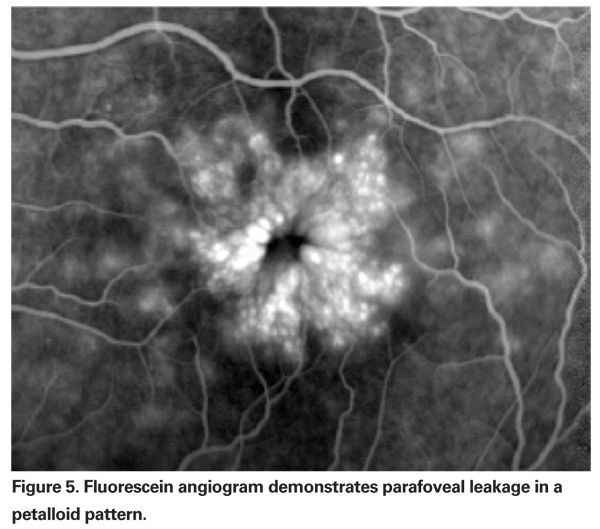
br>Prevenção
Existiram várias revisões retrospectivas e ensaios prospectivos que avaliaram o efeito da profilaxia não profilácticamedicamentos anti-inflamatórios esteróides nas taxas PCME quando usados no pré-operatório versus no pós-operatório. Num relatório, três dias de pré-tratamento com ketorolac trometamina (Acular) foi superior às gotas dadas uma hora antes da cirurgia.6 Quando comparado com o tratamento apenas com corticosteróides pós-operatórios, outro grupo relatou uma redução na PCME de 12% para 0% com dois dias de diclofenaco de sódio (Voltaren) pré-operatório e diclofenaco/corticóide combinado no pós-operatório.5
br>>Utilizando o TOC para quantificar o volume macular, os investigadores descobriram que dois dias de pré-tratamento com cetorolaco e terapia combinada pós-operatória usando cetorolaco/esteróide levaram a uma redução de 46 por cento no inchaço macular um mês após a cirurgia, quando comparado com um grupo de controlo só de esteróides.7 Recentemente, um ensaio prospectivo randomizado comparando três dias de cetorolaco pré-operatório e terapia combinada apenas com corticosteróide relatou que, com base na TOC, os pacientes do grupo de controlo tinham uma incidência de 2,4% de PCME em comparação com 0% na coorte combinada.8 Embora os pacientes do grupo dos corticosteróides tivessem uma incidência significativamente maior de espessamento da retina ≥15 µm, não houve diferença estatística na acuidade visual melhor corrigida entre os dois grupos quatro semanas após a cirurgia.
 br> Numa avaliação prospectiva de três grupos atribuídos à indometacina tópica durante três dias pré-operatórios, seguida de terapia de combinação, apenas terapia de combinação pós-operatória, ou apenas corticosteróide, a incidência de PCME angiográfico foi reduzida de 32.8% (apenas corticosteróides) para 15% (combinação pós-operatória) para 0% (AINE pré e pós-operatório).9
br> Numa avaliação prospectiva de três grupos atribuídos à indometacina tópica durante três dias pré-operatórios, seguida de terapia de combinação, apenas terapia de combinação pós-operatória, ou apenas corticosteróide, a incidência de PCME angiográfico foi reduzida de 32.8% (apenas corticosteróides) para 15% (combinação pós-operatória) para 0% (AINE pré e pós-operatório).9
br>Outro relatório declarou que a adição de nepafenac sódio (Nevanac) a um regime pós-operatório de corticosteróides reduziu as taxas de PCME de 2,1% para 0% quando comparado com corticosteróides apenas.10 Uma recente comparação prospectiva aleatória recente de diclofenaco sozinho versus betametasona no pós-operatório revelou que, cinco semanas após a cirurgia, a incidência de EMC angiográfica era menor no grupo dos AINE (18,8%) do que no grupo dos corticosteróides (58,0%).11
 br> Estes estudos mostram que a utilização profiláctica de AINEs reduz a incidência de PCME, e que a sua eficácia é maior quando iniciada pelo menos três dias antes da cirurgia e continuada durante várias semanas após a mesma. No entanto, o momento exacto e a duração do tratamento pré-operatório e pós-operatório, e a identificação dos pacientes que mais beneficiariam, permanecem ainda indeterminados.
br> Estes estudos mostram que a utilização profiláctica de AINEs reduz a incidência de PCME, e que a sua eficácia é maior quando iniciada pelo menos três dias antes da cirurgia e continuada durante várias semanas após a mesma. No entanto, o momento exacto e a duração do tratamento pré-operatório e pós-operatório, e a identificação dos pacientes que mais beneficiariam, permanecem ainda indeterminados.
br>Características de alto risco
Como mencionado anteriormente, numa série de 1,659 casos consecutivos, membrana epiretinal, um historial de oclusão das veias ou uso pré-operatório de análogos de prostaglandina aumentaram grandemente o risco de desenvolvimento de PCME.4 Ao examinar uma série de pacientes consecutivos encaminhados para uma clínica de retina para gestão de PCME, outro grupo encontrou características de alto risco de diabetes mellitus, hipertensão, cirurgia ocular anterior, membrana epirretínica e extracção complicada de cataratas. (Heier JS, et al.) Dado que uma variedade de doenças médicas e oculares pode predispor os pacientes ao desenvolvimento da PCME, a identificação destes pacientes e a terapia profiláctica agressiva com AINEs tópicos deve ser utilizada para reduzir o risco de desenvolvimento da PCME.
br>Tratamentos
– AINEs. Esta classe de medicamentos inibe a produção de prostaglandinas através da inibição da via do COX (Ver Figura 1). Como os AINE não têm efeito sobre os níveis de prostaglandinas pré-formadas ou existentes, o tratamento antes do trauma cirúrgico é essencial. Num artigo de revisão recente, o autor recomendou tratamento pré-operatório com AINS durante dois dias em pacientes de baixo risco e uma semana para pacientes de alto risco, com continuação pelo menos durante quatro semanas de pós-operatório em ambos os grupos.12
br> Ainda existem perguntas sobre qual AINSID é mais eficaz na prevenção ou tratamento da PCME.
AIDS de nova geração, como o bromfenaco de sódio (Xibrom) e o nepafenaco, têm modificações na sua estrutura química, aumentando a sua penetração ocular e potência teórica.13 Os ensaios in vitro descobriram que a potência relativa da inibição do COX-2 é 18 vezes maior para o bromfenaco do que para o cetorolaco, embora o significado clínico destes dados seja desconhecido.14 Um estudo da farmacocinética in vivo revelou que as concentrações de humor aquoso do nepafenaque comercialmente disponível (nepafenaque mais amfenaco) é significativamente maior do que o do bromfenaco ou do cetorolaco.15 No entanto, não se sabe se estas diferenças de penetração se traduzem em melhores resultados clínicos. Embora numerosas alegações de marketing tenham sido feitas para implicar que a melhor penetração, as mudanças estruturais e a maior potência proposta dos AINE de nova geração se traduzem numa maior eficácia clínica, nenhum estudo definitivo foi feito para confirmar isto.
– Terapia Combinada. Um ensaio prospectivo randomizado, com dupla marcação, avaliando ketorolac versus prednisolona versus terapia combinada para PCME clinicamente significativo, descobriu que os pacientes que receberam terapia combinada alcançaram uma mudança média de ≥2 linhas de visão na sua segunda visita, enquanto os pacientes dos dois grupos de monoterapia nunca alcançaram uma melhoria média de duas linhas no seguimento de três meses.16 Os pacientes tratados com terapia combinada ou apenas com ketorolac também responderam mais rapidamente do que os pacientes do grupo de prednisolona.
br>- Injecções de corticosteróides. Os corticosteróides funcionam mais a montante na mesma via que os AINS, inibindo a libertação de ácido araquadónico dos fosfolípidos de membrana celular, impedindo assim a formação de leucotrienos e prostaglandinas (Ver Figura 1).
Debate continua relativamente à via de administração mais eficaz (sub-Tenon’s versus intravitreal), dosagem óptima (4 mg versus maior), e segurança do doente (riscos de hipertensão ocular, descolamento da retina, hemorragia vítrea e endoftalmite).
Correntemente, não existem ensaios clínicos aleatórios avaliando estes modos de tratamento, e os resultados publicados parecem contraditórios.
br>Um grupo de investigadores descobriu que a triamcinolona intravitreal para PCME persistente resultou numa acuidade visual melhorada, na diminuição da espessura macular e no aumento dos valores de electroretinograma multifocal.17 Outro grupo relatou que a utilização de 4 mg de IVTA em PCME refractária crónica resultou numa melhoria anatómica e funcional após um mês da injecção e persistiu durante pelo menos três meses.18 Contudo, o efeito benéfico foi temporário, uma vez que a acuidade visual e a espessura macular voltaram aos níveis de pré-injecção apesar dos tratamentos múltiplos. Ainda noutra pequena série, os pacientes mantiveram uma melhoria da acuidade e diminuíram a espessura macular após uma dose única de 4 mg IVTA para PCME refractário.19
– Acetazolamida. A acetazolamida aumenta o transporte de fluido subretinal e tem demonstrado remover edema cistóide fetal em doenças como a retinite pigmentosa, afáquia e formação de membrana epiretinal macular.20-23 Há alguns relatos de casos que correlacionam a resolução da PCME com a utilização de acetazolamida oral, mas até à data, não foram realizados ensaios clínicos.
– Agentes anti-vasculares endoteliais do factor de crescimento. O trauma cirúrgico leva à inflamação pós-inflamatória que pode levar à PCME através de um aumento da produção de factores vasopermeáveis como o factor de crescimento endotelial vascular. Mais uma vez, pequenas séries de casos fornecem provas contraditórias. Após a injecção intravitreal com bevacizumab (Avastin), um grupo descobriu que 71% dos doentes ganharam duas ou mais linhas de visão ETDRS;24 e outro relatou que todos os olhos das suas séries tiveram uma melhoria estatisticamente significativa na visão.25 Contudo, outro estudo relatou que o bevacizumab intravitreal não melhorou a acuidade visual em doentes com PCME.26
br>- Vitrectomia. A vitrectomia plana pars com descamação de membrana pode ser considerada em casos de PCME com um componente mecânico identificado quer em exame clínico quer por OCT, ou em casos de edema crónico refractário não responsivo à terapia médica. Numa pequena série, a intervenção cirúrgica resultou numa melhoria superior a três linhas na acuidade visual melhor corrigida na maioria dos pacientes, e na resolução da PCME em todos os casos.27 Há também relatos de casos na literatura que indicam uma melhoria visual após vitrectomia e descamação da membrana limitadora interna.28 Como mencionado anteriormente, a vitrectomia plana pars deve ser considerada em casos de retenção de fragmentos de lente, malposição IOL ou infecção por P. acnes.
br>Direcções Futuras
Como mencionado anteriormente, os corticosteróides funcionam no início da cascata inflamatória. Posurdex (Allergan) é um sistema de administração de dexametasona sustentada biodegradável que é implantado na cavidade vítrea. A sua matriz polimérica transforma-se gradualmente em ácido láctico e glicólico, que por sua vez são decompostos em água e dióxido de carbono. Num estudo de Fase II, 54% dos pacientes que sofrem de PCME e Uveitis-associado a CME mostraram uma melhoria de pelo menos 10 letras de acuidade no dia pós-implante 90, em comparação com apenas 14% mostrando um resultado semelhante no grupo de observação.
br>Recentemente, a FDA aprovou Triesence (Alcon), acetonida de triamcinolona, para injecção intravitreal durante a cirurgia. Este fármaco pode ser utilizado off-label no algoritmo de tratamento da PCME recalcitrante.
É evidente que a definição de PCME tem vindo a evoluir ao longo dos últimos anos. Com aproximadamente 3 milhões de cirurgias de cataratas realizadas nos Estados Unidos por ano e expectativas crescentes dos pacientes, é importante para os especialistas da retina compreender a patogénese variada, os factores de risco e a gestão adequada da PCME. A nova tecnologia revolucionou e irá revolucionar o diagnóstico, prognóstico e tratamento desta patologia.
Os autores praticam na Retinal Consultants do Arizona, Phoenix. O Dr. Jamal também pratica na Texas Retina Associates, Dallas, e o Dr. Goldenberg pratica na Associated Retinal Consultants, Royal Oak, Michigan. Contacte o Dr. Dugel em pdugel @gmail.com.
1. Irvine SR. Uma nova síndrome vítrea definida após cirurgia de catarata. Am J Ophthalmol 1953; 36:599-619.
2. Gass JD, Norton EW. Estudo de seguimento do edema macular do cistoide após a extracção da catarata. Trans Am Acad Ophthalmol Otolaryngol 1969;73(4):665-82.
3. Wright PL, Wilkinson CP, Balyeat HD, et al. Edema angiográfico de cistoide macular após implantação de lentes de câmara posterior. Arch Ophthalmol 1988;106:740-744.
4. Henderson BA, Kim JY, Ament CS, et al. Edema pseudofáfico clínico de cistoide macular. Factores de risco para o desenvolvimento e duração após tratamento. J Cataract Refract Surg 2007;33:1550-8.
5. McColgin AZ, Raizman MB. Eficácia da Voltaren tópica na redução da incidência de edema macular cistóide pós-operatório. Invest Ophthmol Vis Sci 1999;40 S289.
6. Donnenfeld ED, Perry HD, Wittpenn JR, et al. Preoperative ketorolac tromethamine 0,4% in phacoemulsification outcomes: Curva farmacocinético-resposta. J Cataract Refract Surg 2006;32:1474-82.
7. Almeida DR, Johnson D, Hollands H, Smallman D, et al. Efeito dos antiinflamatórios profilácticos não esteróides no edema macular de cistoide avaliado utilizando tomografia de coerência óptica quantificação do volume macular total após cirurgia de catarata. J Cataract Refract Surg 2008;34:64-9.
8. Wittpenn JR, Silverstein S, Heier J, et al. A Randomized, Masked Comparison of Topical Ketorolac 0,4% Plus Steroid vs Steroid Alone in Low-Risk Cataract Surgery Patients. Am J Ophthalmol 2008; 146:554 -560.
9. Yavas GF, Oztürk F, Küsbeci T. Indometacina tópica pré-operatória para prevenir edema macular de cistoide pseudofácico. J Cataract Refract Surg 2007;33:804-7.
10. Wolf EJ, Braunstein A, Shih C, et al. Incidência de edema macular pseudo-fáquico visualmente significativo após uma facoemulsificação rotineira em pacientes tratados com nepafenac. J Cataract Refract Surg 2007;33:1546-1549.
11. Asano S, Miyake K, Ota I, et al. Redução do edema macular angiográfico de cistoides e ruptura da barreira hemato-aquosa após pequena incisão de facoemulsificação e implantação de lentes intra-oculares dobráveis: Comparação multicêntrica prospectiva randomizada de diclofenaco tópico 0,1 por cento e betametasona 0,1 por cento. J Catarata Refract Surg 2008;34:57-63.
12. O’Brien TP. Directrizes emergentes para a utilização da terapia NSAID para optimizar o tratamento de pacientes de cirurgia de catarata. Curr Med Res & Opinião. 2005;21:1131-1137.
13. Walsh DA, Moran HW, Shamblee DA, et al. Agentes anti-inflamatórios 3. Síntese e avaliação farmacológica do ácido 2-amino-3-benzoyl-fenilfenilacético e análogos. J Medicinal Chem 1984;27:1379-1388.
14. Waterbury LD, Silliman D, Jolas T. Comparação da actividade inibitória da ciclo-oxigenase e efeitos anti-inflamatórios oculares da cetorolac trometamina e bromfenac sódio. Curr Med Res Opinião 2006;22: 1133-1140.
15. Walters TR, Raizman M, Ernest P, et al. Farmacocinética in vivo e farmacodinâmica in vitro do nepafenac, amfenac, ketorolac, e bromfenac. J Cataract Refract Surg 2007;33;1539-1545.
16. Heier JS, Topping TM, Baumann W, et al. Ketorolac versus prednisolona versus terapia combinada no tratamento de edema macular pseudofáfico agudo de cistoide. Ophthalmology 2000;107:2034-8.
17. Koutsandrea C, Moschos MM, Brouzas D, et al. Acetonida de triamcinolona intra-ocular para edema macular pseudo-fáquico de cistoide: Estudo de tomografia de coerência óptica e electrooretinografia multifocal. Retina 2007;27:159-64.
18. Boscia F, Furino C, Dammacco R, et al. Intravitreal triamcinolone acetonide in refractory pseudophakic cystoid macular edema: Resultados funcionais e anatómicos. Eur J Ophthalmol 2005;15:89-95.
19. Karacorlu M, Ozdemir H, Karacorlu S. Acetonida de triamcinolona intra-vitreal para o tratamento de edema cistóide macular pseudofáfico crónico. Acta Ophthalmol Scand 2003;81:648-52.
20. Marmor MF. Hipótese relativa ao tratamento com anidrase carbónica de CME: Exemplo com membrana epiretinal. Arch Ophthalmol 1990;108:1524-1525.
21. Cox SN, Hay E, Bird AC. Tratamento de edema macular crónico com acetazolamida. Arch Ophthalmol 1988;106:1190-1195.
22. Fishman GA, Gilbert COT, Fiscella RG et al. Acetazolamida para tratamento de edema macular crónico na retinite pigmentosa. Arch Ophthalmol 1989;107:1445-1452.
23. Wolfensberger TJ, Chiang R, Takeuchi A et al. A inibição da anidrase carbónica ligada à membrana aumenta a absorção do fluido subretinal e a aderência da retina. Graefe’s Arch Clin Exp Ophthalmol 2000; 238:76-80.
24. Arevalo JF, Garcia-Amaris RA, Roca JA, et al. Bevacizumab primário intravitreal para a gestão de edema macular pseudo-fáquico de cistoides: Estudo-piloto do Grupo de Estudo Colaborativo Pan-Americano de Retina. J Cataract Refract Surg. 2007;33:2098-105.
25. Barone A, Russo V, Prascina F, et al. Short-term safety and efficacy of Intravitreal Bevacizumab for Pseudophakic Cystoid Macular Edema. Retina 2008 Oct 9.
26. Spitzer MS, Ziemssen F, Yoeruek E, et al. Eficácia do bevacizumab intravitreal no tratamento do edema cistoide macular pseudofáfico pós-operatório. J Cataract Refract Surg 2008;34:70-5.
27. Pendergast SD, Margherio RR, Williams GA, et al. Vitrectomia para edema cistóide macular crónico pseudofácico. Am J Ophthalmol 1999;128:317-23.
28. Peyman GA, Canakis C, Livir-Rallatos C, et al. The effect of internal limit membrane peeling on chronic recalcitrant pseudophakic cystoid macular edema: Um relatório de dois casos. Am J Ophthalmol 2002;133:571-2.