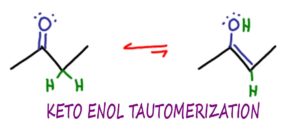
 Die Keto-Enol-Tautomerisierung oder KET ist eine Reaktion in der organischen Chemie, bei der Keton- und Enolmoleküle isomerisieren oder sich gegenseitig umwandeln können, typischerweise in einer säure- oder basenkatalysierten Reaktion.
Die Keto-Enol-Tautomerisierung oder KET ist eine Reaktion in der organischen Chemie, bei der Keton- und Enolmoleküle isomerisieren oder sich gegenseitig umwandeln können, typischerweise in einer säure- oder basenkatalysierten Reaktion.
Die Keto-Enol-Tautomerisierung wird in Ihrem Kurs der organischen Chemie einige Male auftauchen, beginnend mit Alkin-Hydratisierungsreaktionen und wieder auftauchend in Ihren fortgeschrittenen (orgo 2) Enolat- und Kondensationsreaktionen.
Die Tautomerisierung ist eine sehr spezifische Art der Isomerisierung,
in diesem Fall die Umwandlung zwischen den Keto- und Enolformen eines Moleküls.

Keto bezieht sich auf die funktionelle Gruppe des Ketons – allerdings ist KET nicht auf JUST-Ketone beschränkt.
Aldehyde, die Ketonen sehr ähnlich sind,
außer einem terminalen Wasserstoff,
können ebenfalls tautomerisiert werden.
 Enol kommt von ‚Ene‘ wie in Alken,
Enol kommt von ‚Ene‘ wie in Alken,
einer Kohlenstoff-Kohlenstoff-Doppelbindung.
Und ‚ol‘ wie in Alkohol – eine OH-Gruppe.
Fühlen Sie sich eingerostet? Schauen Sie sich die Funktionsgruppen der Organischen Chemie an
Die Tautomerie ist wie die Isomerisierung,
Denken Sie an Tautomere als Isomere, speziell Konstitutionsisomere.
Der Begriff Tautomere bezieht sich auf die zwei spezifischen Formen des Moleküls, die sich im Gleichgewicht umwandeln können.
Bei der KET sind die Keto- und die Enolform Tautomere voneinander.

Welches ist stabiler, Keto oder Enol?
Obwohl es sich um eine reversible Reaktion handelt, ist die Ketoform stabiler und damit vom Gleichgewicht begünstigt.
Das liegt daran, dass ein Kohlenstoff, der doppelt an Sauerstoff gebunden ist, stabiler ist als ein Kohlenstoff, der einfach an Sauerstoff und einfach an Wasserstoff gebunden ist.
Glücklicherweise stammt diese Mathematik aus der Thermodynamik, die bereits in der allgemeinen Chemie behandelt wurde, und ist etwas, das man in der organischen Chemie nicht berechnen muss (manche Professoren verlangen es aber trotzdem).
Das ist keine feste Regel.
Es gibt einige Situationen, in denen die Enolform dem Gesamtmolekül mehr Stabilität verleiht. Schauen Sie sich das folgende Beispiel an:

Die Keto-Form hat ein stabileres Carbonyl, aber die Enol-Form erlaubt es der pi-Bindung, Teil eines viel stabileren aromatischen Systems zu sein (siehe Aromatizität hier). Daher wird die Enolform dieses Moleküls im Gleichgewicht vorherrschen.
Die Keto-Enol-Tautomerisierung kommt in verschiedenen organischen Reaktionen vor, angefangen bei der Hydroborierung und Oxymercurierung von Alkinen.
KET bei der Oxymercurierung von Alkinen
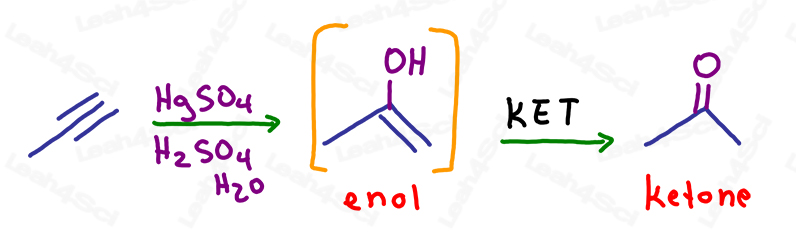
Wie bei den Alkenen wird bei der Oxymercurierungsreaktion einfach EINE pi-Bindung gebrochen, um einen Alkohol an das stärker substituierte Kohlenstoffatom zu addieren, gemäß der Markovnikov-Regel.
Das resultierende Molekül hat noch eine pi-Bindung: ein Alken am gleichen Kohlenstoff wie der Alkohol.
Dies ist ein instabiles Enol und wird automatisch eine Keto-Enol-Tautomerisierung durchlaufen, um ein stabileres Keton-Endprodukt zu bilden.
KET bei der Hydroboration von Alkinen
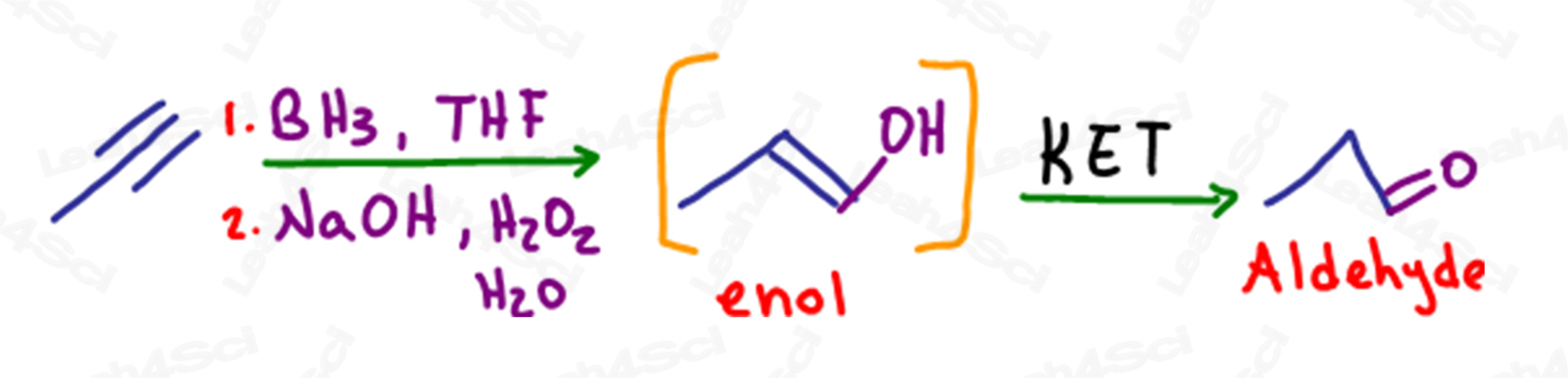
Wie bei den Alkenen ist die Hydroboration eine Anti-Markovnikov-Reaktion, bei der eine pi-Bindung gebrochen und ein Alkohol an den weniger substituierten Kohlenstoff angehängt wird.
Im Fall eines endständigen Alkins, wenn eine einzelne pi-Bindung in einen Alkohol umgewandelt wird, hat der endständige Kohlenstoff immer noch eine pi-Bindung oder ein Alken, was es zu einem Enol macht.
Dieses Molekül wird auch eine Tautomerisierung durchlaufen, um ein stabileres Aldehydprodukt zu bilden.
Trotz der Bildung eines Aldehyds wird diese Reaktion immer noch als Keto-Enol-Tautomerisierung betrachtet.
Für diese beiden Reaktionen wird das resultierende Keton oder Aldehyd durch die Position des Enols bestimmt.
Wenn das Enol an einem internen (nicht-terminalen) Kohlenstoff ist, wird das resultierende Produkt ein Keton bilden.
Ist das Enol endständig, dann wird das resultierende Carbonyl ein Aldehyd sein.
Die Tautomerisierung kann sowohl unter säurekatalysierten als auch unter basenkatalysierten Bedingungen stattfinden.
Betrachten Sie bei den obigen Reaktionen, wie die Bedingungen nach der Hydratisierung sein müssen.
Das folgende Video führt Sie Schritt für Schritt durch
- Säure-katalysierte Tautomerisierungsreaktion und Mechanismus
- Base-katalysierte Tautomerisierungsreaktion und Mechanismus
- Die umgekehrte Reaktion (Keto- zu Enolform) für beide Reaktionen
Säure-.Katalysierte Tautomerisierung – Mechanismus im Überblick
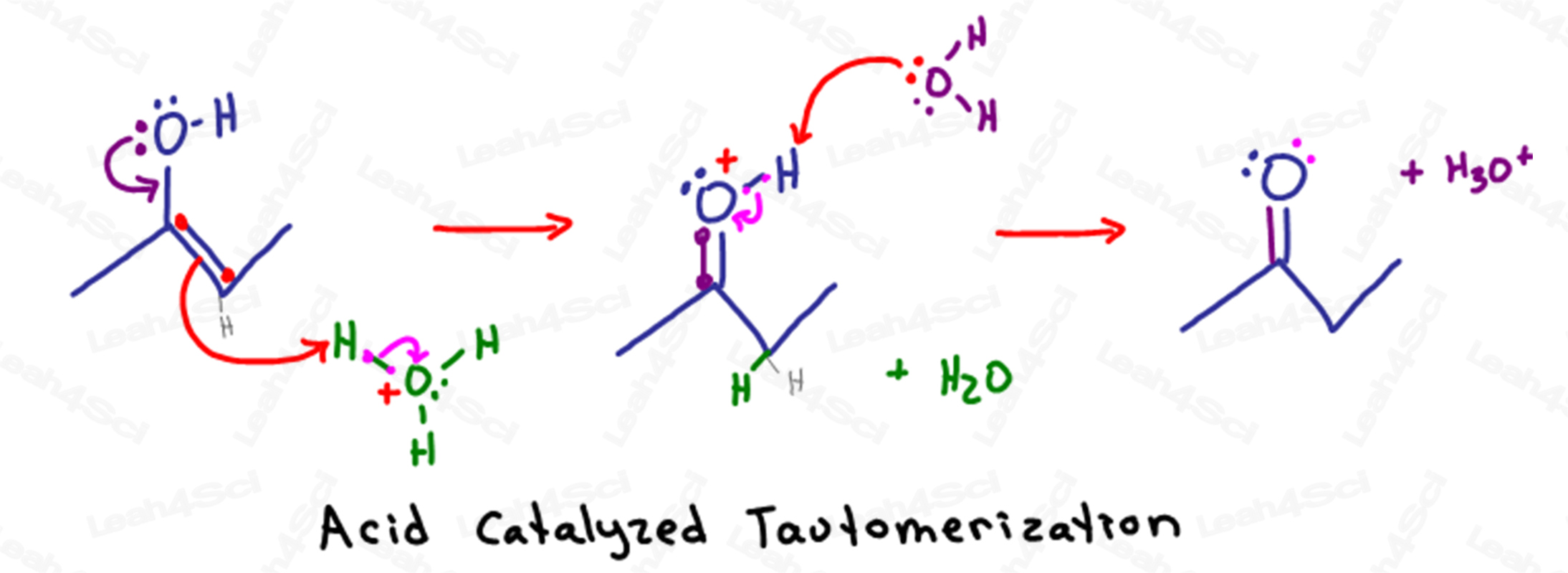
Erinnern Sie sich, dass in sauren wässrigen Lösungen viel Wasser und Hydronium (H3O+) in Lösung vorliegt.
Die Tautomerisierung beginnt, wenn die teilweise negativen Elektronen am Sauerstoff des Alkohols nach unten reichen, um das sp2-Kohlenstoffatom (dasjenige, das die pi-Bindung hält) anzugreifen.
Bei der Bildung einer zweiten Bindung zwischen Kohlenstoff und Sauerstoff würde der Kohlenstoff insgesamt 5 Bindungen haben.
Um sein Oktett nicht zu verletzen, stößt der Kohlenstoff die pi-Bindung zwischen sich und dem anderen sp2-Kohlenstoffatom heraus und schiebt die Elektronen auf das andere Kohlenstoffatom.
Anstatt als einsames Paar auf dem Kohlenstoff zu sitzen, werden die negativen Elektronen von dem teilweise positiven H+-Atom auf einem nahe gelegenen Hydroniummolekül angezogen.
Da dieses H+-Atom nur eine Bindung haben kann, lässt es die Elektronen los, die es an den Sauerstoff binden, so dass das Wasser in Lösung geht.
Das resultierende Molekül sieht wie ein Keton aus, mit Ausnahme des instabilen Sauerstoffatoms.
Sauerstoff, mit zwei Bindungen an den Kohlenstoff, einer Bindung an den Wasserstoff und einem einzelnen einsamen Paar, hat eine instabile positive Ladung.
Ein weiteres Wassermolekül in Lösung nutzt seine teilweise negativen Elektronen, um den Sauerstoff zu deprotonieren und somit seine Elektronen zurückzugeben, um ein neutrales, stabiles Keton zu bilden.
Lassen Sie uns eine kurze Rechnung aufstellen.
Diese Reaktion begann, als das Enol das Hydronium, unseren sauren Katalysator, angriff.
Im letzten Schritt deprotoniert Wasser das Keton und reformiert unseren Hydronium-Säurekatalysator.
Erinnerung: wenn das Enol endständig ist, ist das resultierende Produkt ein Aldehyd anstelle eines Ketons
Base-katalysierte Tautomerisierung – Überblick über den Mechanismus
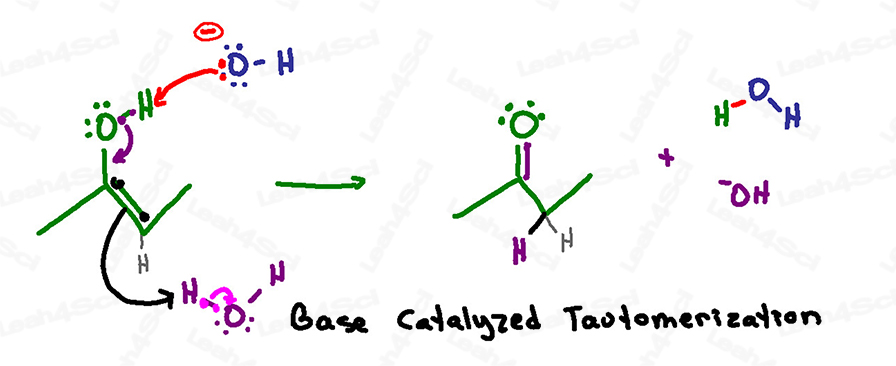
Erinnerung: in einer basischen wässrigen Lösung haben wir sowohl Hydroxid als auch Wasser herumschwimmen.
Niemals H+ oder Hydronium in einer basischen Lösung zeigen!
Diese Reaktion ist dem säurekatalysierten Mechanismus sehr ähnlich, außer dass die Deprotonierung der erste und nicht der letzte Schritt ist.
Das liegt daran, dass die basische Lösung mit einem negativen Sauerstoff umgehen kann, aber die saure Lösung keinen negativen Sauerstoff entstehen lässt.
Diese Reaktion beginnt, wenn ein basisches Hydroxid in Lösung nach dem sauren Wasserstoff am Enol greift.
Anstatt zurück auf den Sauerstoff zu kollabieren, um ein negatives Oxid zu bilden, kollabieren die Elektronen schnell nach unten, um eine Carbonyl-pi-Bindung zwischen Kohlenstoff und Sauerstoff zu bilden.
Wie bei dem säurekatalysierten Mechanismus muss der Kohlenstoff seine aktuelle Doppelbindung ausstoßen, um zu vermeiden, dass er 5 Bindungen hat und sein Oktett verletzt.
Die pi-Bindungselektronen sitzen nicht auf dem anderen Kohlenstoff und warten, stattdessen suchen sie sich ein Proton aus der Lösung – und schnappen es sich von einem Wassermolekül.
In einer einzigen Angriffsreihe (einem Schritt) haben wir ein Keton als unser Endprodukt.
Achten Sie darauf, was in dieser Reaktion verwendet und reformiert wurde:
Hydroxid schnappte sich ein Proton und bildete Wasser,
Aber das Enol schnappte sich ein Proton aus dem Wasser und bildete Hydroxid und reformierte so den basischen Katalysator, der diese Reaktion einleitete.
Erinnerung: Wenn das Enol endständig ist, ist das resultierende Produkt ein Aldehyd statt ein Keton