Addition an Alkene
NBS reagiert mit Alkenen 1 in wässrigen Lösungsmitteln zu Bromhydrinen 2. Die bevorzugten Bedingungen sind die portionsweise Zugabe von NBS zu einer Lösung des Alkens in 50 % wässrigem DMSO, DME, THF oder tert-Butanol bei 0 °C. Die Bildung eines Bromonium-Ions und der sofortige Angriff durch Wasser führt zu starken Markovnikov-Additionen und antistereochemischen Selektivitäten.

Nebenreaktionen umfassen die Bildung von α-Bromketonen und Dibromverbindungen. Diese können durch die Verwendung von frisch umkristallisiertem NBS minimiert werden.
Mit der Zugabe von Nukleophilen, anstelle von Wasser, können verschiedene bifunktionelle Alkane synthetisiert werden.

Allylische und benzylische BromierungBearbeiten
Standardbedingungen für die Verwendung von NBS in allylische und/oder benzylische Bromierung beinhaltet das Rückflussen einer Lösung von NBS in wasserfreiem CCl4 mit einem Radikalinitiator – üblicherweise Azobisisobutyronitril (AIBN) oder Benzoylperoxid, Bestrahlung oder beides, um die radikalische Initiierung zu bewirken. Die Allyl- und Benzylradikal-Zwischenprodukte, die während dieser Reaktion gebildet werden, sind stabiler als andere Kohlenstoffradikale und die Hauptprodukte sind Allyl- und Benzylbromide. Dies wird auch als Wohl-Ziegler-Reaktion bezeichnet.

Der Tetrachlorkohlenstoff muss während der gesamten Reaktion wasserfrei gehalten werden, da die Anwesenheit von Wasser das gewünschte Produkt wahrscheinlich hydrolysiert. Bariumcarbonat wird oft hinzugefügt, um wasserfreie und säurefreie Bedingungen aufrechtzuerhalten.
In der obigen Reaktion ist zwar ein Gemisch von isomeren Allylbromidprodukten möglich, aber aufgrund der größeren Stabilität des Radikals in 4-Position gegenüber dem methylzentrierten Radikal entsteht nur eines.
Bromierung von CarbonylderivatenEdit
NBS kann Carbonylderivate entweder über einen radikalischen Weg (wie oben) oder über Säurekatalyse α-bromieren. Zum Beispiel kann Hexanoylchlorid 1 in der alpha-Position durch NBS unter Verwendung von Säurekatalyse bromiert werden.

Die Reaktion von Enolaten, Enolethern oder Enolacetaten mit NBS ist die bevorzugte Methode der α-Bromierung, da sie sehr ertragreich ist und nur wenige Nebenprodukte erzeugt.
Bromierung von aromatischen Derivaten
Elektronenreiche aromatische Verbindungen, wie Phenole, Aniline und verschiedene aromatische Heterocyclen, können mit NBS bromiert werden. Die Verwendung von DMF als Lösungsmittel ergibt eine hohe Para-Selektivität.
Hofmann-UmlagerungEdit
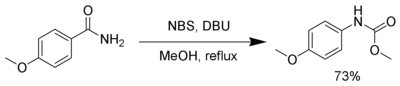
NBS reagiert in Gegenwart einer starken Base, wie DBU, mit primären Amiden unter Bildung eines Carbamats über die Hofmann-Umlagerung.
Selektive Oxidation von AlkoholenEdit
Es ist ungewöhnlich, aber möglich, dass NBS Alkohole oxidiert. E. J. Corey et al. fanden heraus, dass man sekundäre Alkohole in Gegenwart von primären Alkoholen mit NBS in wässrigem Dimethoxyethan (DME) selektiv oxidieren kann.
