Rédacteurs initiaux – Alex Kent du projet Pathophysiologie des problèmes complexes des patients de l’Université Bellarmine.
Principaux contributeurs – Alex Kent, Gayatri Jadav Upadhyay, Elaine Lonnemann, Kim Jackson et Wendy Walker
Définition/Description
L’acromégalie est une maladie systémique rare qui affecte l’ensemble du corps. Elle se caractérise par une hypersécrétion d’hormone de croissance (GH) que l’organisme est incapable de réguler. La GH facilite la croissance des muscles, des organes internes et des os, et stimule la sécrétion de son hormone cible, le facteur de croissance insulinique 1 (IGF-1). Les niveaux extrêmement élevés de GH et d’IGF-1 qui caractérisent l’acromégalie provoquent une hypertrophie des tissus et des changements métaboliques qui entraînent des déformations visibles ainsi qu’une augmentation de la mortalité. La maladie débute souvent entre 30 et 50 ans, et a un début insidieux et une progression lente, ce qui retarde souvent le diagnostic jusqu’à des stades plus avancés de la maladie.

Prévalence
- La prévalence de l’acromégalie est d’environ 40 à 70 cas par million de personnes.
- Toutefois, de nouvelles recherches suggèrent que la prévalence pourrait atteindre 77 cas par million de personnes.
- L’incidence annuelle de l’acromégalie est d’environ est de 3-4 nouveaux cas par million de personnes.
Caractéristiques/Présentation clinique
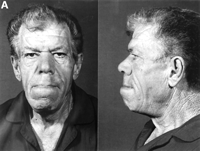
L’acromégalie affecte de nombreux systèmes de l’organisme, et divers signes et symptômes se développent sur une période de plusieurs années. Ils vont de changements subtils à une défiguration notable. Les caractéristiques communes sont : :
- Grandissement des mains et des pieds
- Hyperhydrose- augmentation de la transpiration
- Augmentation de l’épaisseur de la peau
- Fombrage et épaississement des poils du corps
- Bossage frontal du crâne-. un front anormalement lourd et un front proéminent
- Élargissement du maxillaire accompagné d’une séparation des dents
- Malocclusion des mâchoires et supraclusion
- Élargissement des tissus mous
- Surcroissance et épaississement du squelette faisant apparaître de nombreuses zones comme enflées
- Voix grave et rauque due à l’épaississement du cartilage dans le larynx
- Dysfonctionnement ventilatoire
- Gain de poids
- Douleurs articulaires
- Apnée du sommeil
- Acné
- Problèmes de vision
.
 |
 |
Comorbidités associées
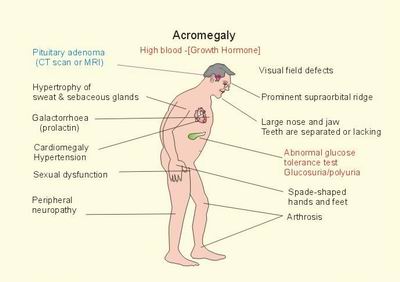
L’IGF-1, la molécule cible de la GH, permet de nombreuses actions de promotion de la croissance de la GH ; la GH elle-même est également un régulateur du métabolisme minéral, lipidique et glucidique. Par conséquent, les taux élevés de GH et d’IGF-1 qui sont caractéristiques de l’acromégalie entraînent une croissance excessive des tissus mous, un gonflement des organes internes et des comorbidités musculo-squelettiques, neurologiques et métaboliques.
Cardiovasculaire :
- Hypertension
- Arrythmie
- Valvulopathie
- Cardiomyopathie
- Hypertrophie (biventriculaire ou septale asymétrique)
- Insuffisance cardiaque congestive
Pulmonaire :
- Apnée obstructive du sommeil
- Macroglossie
- Obstruction des voies aériennes supérieures
- Dysfonctionnement ventilatoire
- Obstruction des voies aériennes supérieures
Métabolique :
- Résistance à l’insuline
- Métabolisme du glucose altéré
- Diabète sucré
Viscéral :
- Grossissement des organes
- Polypes du côlon
- Rétention des liquides
- Insuffisance rénale
Musculo-squelettique :
- Arthropathie/arthrose
- Syndrome du canal carpien
- Osteopénie
Médicaments
- Analogues de la somatostatine- la somatostatine inhibe les cellules endocrines, notamment les cellules sécrétrices de GH de l’hypophyse. Les analogues de la somatostatine (SSA) imitent les effets de suppression de la GH de la somatostatine de l’organisme. Les ASA sont l’un des médicaments les plus couramment prescrits pour l’acromégalie. Trois SSA sont actuellement approuvés aux États-Unis : octréotride à action brève, octréotride LAR et Somatuline Depot. Les effets indésirables les plus fréquents sont l’intolérance au glucose et les calculs de la vésicule biliaire et des boues.
- Agonistes de la dopamine- entraîne une suppression de la GH chez une partie des patients acromégales. Il est intéressant de noter que ce médicament stimule la libération de GH chez les patients sains. Les avantages de ce médicament sont un coût relativement faible, une administration orale et l’absence d’hypopituitarisme associé au médicament. Cependant, le médicament n’est efficace que pour abaisser la GH et l’IGF-1 à des niveaux sûrs chez environ 10% des patients, et provoque potentiellement des lésions valvulaires cardiaques.
- Agonistes des récepteurs de l’hormone de croissance- bloque le signal de la GH pour la production d’IGF-1. Plus efficaces pour les patients ayant des niveaux plus élevés d’IGF-1, et ont démontré une influence plus favorable sur le contrôle glycémique. Les effets indésirables souvent associés aux agonistes des récepteurs de l’hormone de croissance sont une fonction hépatique compromise et des réactions au site d’injection.
Tests diagnostiques/Tests de laboratoire/Valeurs de laboratoire

Test de tolérance au glucose oral (TTGO) – le glucose a un signal suppressif neuroendocrinien qui abaisse la GH. Dans ce test, 75 g de glucose sont administrés avec des mesures de GH à différents points sur une période de 120 minutes. L’incapacité à supprimer la sécrétion de GH à moins de 1 microgramme/litre est actuellement la norme pour le diagnostic de l’acromégalie.
Imagerie par résonance magnétique (IRM) – la méthode d’imagerie privilégiée lors du diagnostic de l’acromégalie. Une IRM de l’hypophyse est réalisée afin de rechercher toute croissance anormale. Elle peut aider à déterminer la taille de la tumeur, ainsi que la compression des structures environnantes.
Tests sanguins – le sang peut être utilisé pour mesurer les niveaux sériques d’IGF-1 en plus de la GH. Des taux élevés d’IGF-1 ont été utilisés comme marqueur de l’acromégalie ; l’IGF-1 est corrélé aux taux de GH ainsi qu’aux manifestations cliniques de l’acromégalie. Les taux d’IGF-1 ont également tendance à rester stables tout au long de la journée, ce qui fait du test d’IGF-1 un outil de diagnostic assez fiable. En général, un diagnostic d’acromégalie peut être exclu si les taux d’IGF-1 se situent dans la fourchette normale.
Radiographies – une radiographie du crâne peut montrer un épaississement osseux ainsi qu’un élargissement des sinus nasaux. Un épaississement des phalanges carpiennes peut être observé sur les radiographies des mains.
Tomographie par ordinateur (CT)- cette méthode d’imagerie peut être utilisée pour identifier des croissances anormales dans l’hypophyse.
Valeurs de laboratoire
Hormone de croissance (GH)- chez les individus sans acromégalie, les valeurs de GH sont généralement de 0,1-0,2 microgrammes/litre. Il y a cependant 6 à 10 salves de sécrétion de GH où les taux de l’hormone sont de 5 à 30 microgrammes/litre. Cela peut recouper les valeurs observées chez les patients atteints d’acromégalie. Des concentrations d’hormone de croissance inférieures à 2,5 ng/ml sont associées à des taux de mortalité similaires à ceux de la population normale. Ainsi, la normalisation des taux de GH est actuellement définie comme étant inférieure à 2,5 ng/ml.


Etiologie/Causes

- La majorité (99%) des cas d’acromégalie sont causés par la prolifération des cellules somatotrophes dans l’hypophyse, ce qui conduit à un adénome hypophysaire. Les cellules somatotrophes constituent plus de la moitié des cellules sécrétrices d’hormones dans l’hypophyse.
- La tumeur hypophysaire provoque une augmentation des taux circulants de GH. La GH médiatise les réactions anaboliques en se liant aux récepteurs de l’hormone de croissance, en créant des sites d’amarrage pour les protéines de signalisation cellulaire et en initiant la synthèse de gènes cibles comme l’IGF-1. Cela augmente à son tour la production du facteur de croissance 1 analogue à l’insuline (IGF-1). L’IGF-1 provoque des changements métaboliques et une croissance somatique, stimulant la prolifération du cartilage, des muscles squelettiques et des os qui conduisent finalement à un élargissement des tissus.
- L’hypertrophie des tissus et les anomalies métaboliques provoquent la multiplication par deux ou trois de la mortalité observée dans l’acromégalie.
Implication systémique
Implication cardiovasculaire
- Cordiomyopathie acromégale- les caractéristiques communes comprennent une hypertrophie biventriculaire, un épaississement des parois cardiaques, un dysfonctionnement diastolique, une fonction systolique limitée et une insuffisance cardiaque avec des signes de cardiomyopathie dilatative.
- Dysfonctionnement des valves mitrale et aortique.
- Arrythmie- liée à une combinaison de facteurs, notamment une augmentation de l’épaisseur de la paroi du ventricule gauche ainsi que des potentiels d’action tardifs dans le cœur.
- Hypertension- due en partie à l’augmentation du volume plasmatique.
- Atherosclérose et dysfonctionnement endothélial
Introduction métabolique
- Tolérance au glucose altérée et diabète sucré- l’hormone de croissance contrecarre les effets de l’insuline sur le métabolisme du glucose. La GH régule également la réponse des tissus à l’insuline ; en conséquence, un excès de GH peut être un facteur causal de la résistance à l’insuline.
- Amoindrissement du métabolisme lipidique- l’acromégalie est corrélée à des anomalies du métabolisme lipidique.Des études ont montré que les niveaux de triglycérides sériques étaient plus élevés chez les patients atteints d’acromégalie.
Implication pulmonaire
- La mortalité associée aux troubles respiratoires a augmenté chez les patients atteints d’acromégalie.
- Incidence accrue des apnées du sommeil.
- Poitrine en tonneau développée en raison de changements dans la morphologie des vertèbres et des côtes. Les côtes s’allongent et les corps vertébraux s’élargissent et s’allongent, ce qui nuit à l’inspiration.
Gestion médicale
Le but de la gestion médicale actuelle est de réduire les effets de la tumeur hypophysaire par une résection chirurgicale, de réguler l’hypersécrétion de GH et d’IGF-1 par des médicaments, de tenter d’améliorer les nombreuses comorbidités associées à la maladie, de réduire le risque de mortalité et de maintenir une fonction normale de l’hypophyse.
Chirurgie

- La chirurgie hypophysaire est souvent le premier choix dans la prise en charge de l’acromégalie car elle permet de réduire l’hypersécrétion de GH et d’IGF-1 et de réduire les effets de la tumeur sur les structures cérébrales environnantes.
- Le but du <span />débridement chirurgical est de réséquer la plus grande partie possible de la tumeur tout en maintenant une fonction normale de l’hypophyse.
- La résection des adénomes de l’hypophyse est difficile en raison de l’emplacement de l’hypophyse et de sa proximité avec d’importantes structures vasculaires et neurales. Par conséquent, la chirurgie est plus réussie avec un chirurgien expérimenté ; de nombreuses études ont démontré que le résultat du traitement chirurgical de l’acromégalie est corrélé au niveau d’expérience du chirurgien.
Traitement médicamenteux
- Analogues de la somatostatine
- Agonistes de la dopamine
- Agonistes des récepteurs de l’hormone de croissance
- Les actions spécifiques de ces médicaments sont décrites dans la section Médicaments.
Radiothérapie
- Implique l’utilisation d’une irradiation à haute tension.
- Moins traumatisant que la chirurgie traditionnelle.
- La radiothérapie est délivrée en doses hebdomadaires réparties sur une période de six semaines.
- Approximativement 50% des patients atteints d’acromégalie connaissent une rémission biochimique après la radiothérapie.
- La radiothérapie peut prendre des années avant de produire son plein effet.
Gestion par la physiothérapie
L’acromégalie est une maladie qui affecte plusieurs systèmes du corps. Les thérapeutes peuvent être appelés à fournir un programme portant sur les manifestations musculo-squelettiques et neurologiques de la maladie.
Modèles de pratique privilégiés :
- 4D : Altération de la mobilité articulaire, de la fonction motrice, de la performance musculaire et de l’amplitude des mouvements associée à un dysfonctionnement du tissu conjonctif.
- 4E : Altération de la mobilité articulaire, de la fonction motrice, de la performance musculaire et de l’amplitude des mouvements associée à une inflammation localisée.
- 4F : Altération de la mobilité articulaire, de la fonction motrice, de la performance musculaire, de l’amplitude des mouvements et de l’intégrité des réflexes associée à des troubles de la colonne vertébrale.
- 5F : Altération de l’intégrité des nerfs périphériques et de la performance musculaire associée à une lésion des nerfs périphériques.
Dépistage
- Les personnes atteintes d’acromégalie doivent faire l’objet d’un dépistage des modifications de la mobilité articulaire, de la diminution de la tolérance à l’exercice et de la faiblesse.
- Si un client acromégale se présente à la physiothérapie avec une faiblesse musculaire inhabituelle, il devrait être référé à un médecin pour un bilan complet à la recherche de neuropathies et de myopathies inflammatoires. Cela permettra d’identifier les causes sous-jacentes qui peuvent être traitées.
Intervention orthopédique
- L’arthrite de plusieurs articulations est souvent présente chez les patients atteints d’acromégalie. En outre, le syndrome du canal carpien est observé chez environ 50 % des patients atteints d’acromégalie, et il existe une incidence similaire de douleurs thoraciques et lombaires chez les patients acromégales.
- Les études radiographiques ont mis en évidence de gros ostéophytes dans le ligament longitudinal antérieur et un espace intervertébral accru.
- Un programme de physiothérapie travaillerait à promouvoir la force musculaire, la mobilité des articulations et l’indépendance avec les activités fonctionnelles. Un équipement adapté pour l’aide aux activités de la vie quotidienne peut être envisagé en fonction de la gravité de la maladie.
Intervention postopératoire
- L’exercice et la déambulation sont encouragés dans les 24 premières heures après l’ablation de la tumeur hypophysaire.
- Des exercices respiratoires sont indiqués. En revanche, la toux, les éternuements et le mouchage sont contre-indiqués.
- Surveillez étroitement les signes vitaux. Tout changement de la vision, une baisse du pouls ou une augmentation de la pression artérielle pourrait indiquer une augmentation de la pression intracrânienne et doit être signalé immédiatement.
- Le kinésithérapeute doit consulter le personnel infirmier pour déterminer si une surveillance de la glycémie est nécessaire pendant l’exercice. Le taux de GH peut chuter rapidement après l’ablation de la tumeur et entraîner une hypoglycémie.
Diagnostic différentiel
Plusieurs des comorbidités de l’acromégalie chevauchent des troubles courants ; par conséquent, l’acromégalie peut être mal diagnostiquée. Les comorbidités qui peuvent conduire à un mauvais diagnostic comprennent :
- Arthrite
- Hypertension
- Diabète sucré
- Syndrome du tunnel carpien
- Dysfonctionnement respiratoire
- Implication cardiaque
- L’échec de la suppression de l’hormone de croissance peut également être observé chez les patients diabétiques, d’insuffisance rénale, d’insuffisance hépatique et de patients souffrant d’obésité ou sous traitement œstrogénique substitutif. Cela pourrait potentiellement conduire à un mauvais diagnostic.
Ressources
- L’Association du réseau hypophysaire. Acromégalie.org. Cliquez ici
- Service national d’information sur les maladies endocriniennes et métaboliques. Cliquez ici
- University of Maryland Medical Center. Cliquez ici
- 1,0 1,1 1,2 1,3 1,4 1,5 1,6 1,7 1. Vance M. Acromégalie : un trouble hypophysaire fascinant. Neurosurg Focus 2010;29(4):1.
- 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 2,13 2,14 2,15 2,16 2,17 2,18 2,19 2,20 2,21 2,22 2,23 2,24 2,25 2,26 2. Cordero RA, Barkan AL. Diagnostic actuel de l’acromégalie. Rev Endocr Metab Disord 2008;9:13-19.
- 3.0 3.1 3.2 3.3 3.4 3.5 3.6 3.7 3.8 3.9 3.Merck Manual Home Edition. Acromégalie et gigantisme : troubles de l’hypophyse. http://www.merckmanuals.com/home/print/sec13/ch162e.html (consulté le 11 mars 2011).
- 4.00 4.01 4.02 4.03 4.04 4.05 4.06 4.07 4.08 4.09 4.10 4.11 4.12 4.13 4.14 4.15 4.16 4.17 4.Fleseriu M, Delashaw JB, Cook DM. Acromégalie : revue de la thérapie médicale actuelle et des nouveaux médicaments à l’horizon. Neurosurg Focus 2010;29(4):E15.
- 5.0 5.1 5.2 5.3 5.4 5.5 5.6 5.7 5.8 5. Reid TJ, Post KD, Bruce JN, Kanibir MN, Reyes-Vidal CM, Freda PU. Les caractéristiques au moment du diagnostic de 324 patients atteints d’acromégalie n’ont pas changé entre 1981 et 2006 : l’acromégalie reste sous-reconnue et sous-diagnostiquée. Endocrinologie clinique 2010;72:203-208.
- 6.00 6.01 6.02 6.03 6.04 6.05 6.06 6.07 6.08 6.09 6.10 6.11 6.12 6.13 6.14 6.15 6.16 6.17 6.18 6.19 6.20 6.21 6.Melmed S. Acromégalie pathogenèse et traitement. J. Clin. Invest 2009;119:3189-3202.
- 7,0 7,1 7,2 7,3 7,4 7,5 7,6 7,7 7,8 7.Del Porto LA, Liubinas SV, Kaye AH. Traitement de l’acromégalie persistante. J Clin Neurosci 2011 ; 18:181-190.
- 8,00 8,01 8,02 8,03 8,04 8,05 8,06 8,07 8,08 8,09 8,10 8,11 8,12 8,13 8,14 8.Colao A, Ferone D, Marzullo P, Lombardi G. Complications systémiques de l’acromégalie : épidémiologie, pathogenèse et gestion. Revues endocriniennes. 2004 ; 25(1):102-152
- 9.00 9.01 9.02 9.03 9.04 9.05 9.06 9.07 9.08 9.09 9.10 9.11 9.12 9.13 9.14 9.15 9.16 9.Goodman CC, Fuller KS. Pathology : implications for the physical therapist. 3rd ed. St.Louis : Saunders-Elsevier, 2009.