Ajout aux alcènesEdit
Le NBS réagira avec les alcènes 1 dans des solvants aqueux pour donner des bromohydrines 2. Les conditions préférées sont l’addition par portions de NBS à une solution de l’alcène dans du DMSO, DME, THF ou tert-butanol aqueux à 50% à 0 °C. La formation d’un ion bromonium et l’attaque immédiate par l’eau donnent une forte addition de Markovnikov et des sélectivités anti stéréochimiques.

Les réactions secondaires comprennent la formation d’α-bromocétones et de composés dibromo. Celles-ci peuvent être minimisées par l’utilisation de NBS fraîchement recristallisé.
Avec l’ajout de nucléophiles, au lieu d’eau, divers alcanes bifonctionnels peuvent être synthétisés.

Bromation allylique et benzyliqueEdit
Conditions standard d’utilisation de la NBS en… bromation allylique et/ou benzylique implique le reflux d’une solution de NBS dans du CCl4 anhydre avec un initiateur de radicaux – généralement de l’azobisisobutyronitrile (AIBN) ou du peroxyde de benzoyle, une irradiation, ou les deux, pour effectuer l’initiation radicalaire. Les intermédiaires radicalaires allyliques et benzyliques formés au cours de cette réaction sont plus stables que les autres radicaux de carbone et les principaux produits sont les bromures allyliques et benzyliques. Cette réaction est également appelée réaction de Wohl-Ziegler.

Le tétrachlorure de carbone doit être maintenu anhydre tout au long de la réaction, car la présence d’eau peut probablement hydrolyser le produit souhaité. Du carbonate de baryum est souvent ajouté pour maintenir des conditions anhydres et sans acide.
Dans la réaction ci-dessus, alors qu’un mélange de produits bromure allylique isomères est possible, un seul est créé en raison de la plus grande stabilité du radical en position 4 par rapport au radical centré sur le méthyle.
Bromation de dérivés carbonylés
La NBS peut α-bromer des dérivés carbonylés via une voie radicalaire (comme ci-dessus) ou via une catalyse acide. Par exemple, le chlorure d’hexanoyle 1 peut être bromé en position alpha par NBS en utilisant la catalyse acide.

La réaction d’énolates, d’éthers d’énol ou d’acétates d’énol avec NBS est la méthode préférée d’α-bromation car elle a un rendement élevé avec peu de produits secondaires.
Bromation de dérivés aromatiquesEdit
Les composés aromatiques riches en électrons, tels que les phénols, les anilines, et divers hétérocycles aromatiques, peuvent être bromés en utilisant le NBS. L’utilisation du DMF comme solvant donne des niveaux élevés de para-sélectivité.
Réarrangement de HofmannEdit
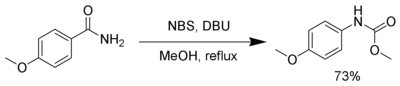
Le NBS, en présence d’une base forte, comme le DBU, réagit avec les amides primaires pour produire un carbamate via le réarrangement de Hofmann.
Oxydation sélective des alcoolsEdit
Il est peu fréquent, mais possible pour NBS d’oxyder les alcools. E. J. Corey et al. ont découvert que l’on pouvait oxyder sélectivement les alcools secondaires en présence d’alcools primaires en utilisant du NBS dans du diméthoxyéthane (DME) aqueux.

.