L’atomo di carbonio elettrofilo delle aldeidi e dei chetoni può essere il bersaglio dell’attacco nucleofilo delle ammine e degli alcoli. Il risultato finale dell’attacco di un nucleofilo amminico è un gruppo funzionale in cui il doppio legame C=O è sostituito da un doppio legame C=N, ed è noto come un’immina. (Un termine equivalente è “base di Schiff”, ma useremo “immina” in tutto il libro). Ricordiamo dalla sezione 7.5B che le immine hanno un pKa di circa 7, quindi a pH fisiologico possono essere accuratamente disegnate come protonate (forma di ione iminio) o neutre (immina).
Formazione dello ione iminio:
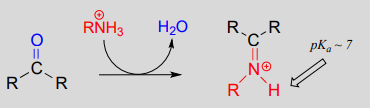
Meccanismo (enzimatico):
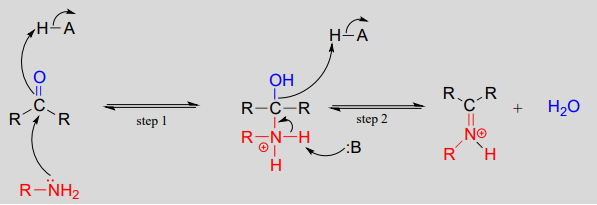
Meccanicamente, la formazione di un’imina comporta due passi. In primo luogo, l’azoto dell’ammina attacca il carbonio carbonilico in un passo di addizione nucleofila (passo 1) che è strettamente analogo alla formazione dell’emiacetale e dell’emiketale. Sulla base della tua conoscenza del meccanismo di formazione dell’acetale e del chetale, potresti aspettarti che il passo successivo sia l’attacco di una seconda ammina per formare un composto con un carbonio legato a due gruppi amminici – la versione azotata di un chetale o acetale. Invece, quello che succede dopo (passo 2 sopra) è che gli elettroni della coppia solitaria di azoto “spingono” l’ossigeno fuori dal carbonio, formando un doppio legame \(C=N\) (un iminio) e una molecola di acqua spostata.
La conversione di un iminio in un’aldeide o in un chetone è un processo idrolitico (i legami sono rotti da una molecola d’acqua), e meccanicamente è semplicemente l’inverso della formazione dell’iminio:
Idrolisi di uno ione iminio:
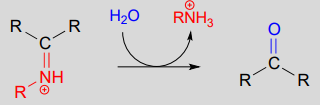
Meccanismo (enzimatico):
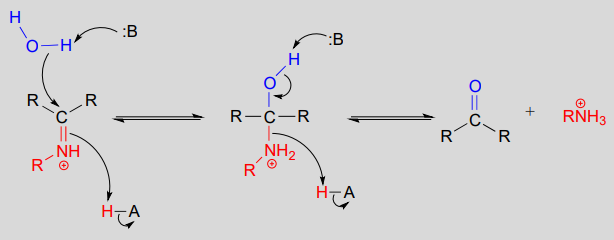
Gli enzimi che formano legami carbonio-carbonio chiamati aldolasi (che copriremo in dettaglio nel capitolo 12) spesso formano legami iminio tra un carbonio carbonile su un substrato e un residuo di lisina dal sito attivo dell’enzima, come in questa reazione aldolasi dal ciclo di Calvin:
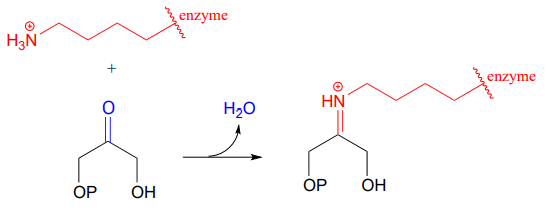
Dopo che il legame carbonio-carbonio che fa parte di una reazione di aldolasi è completato, il legame iminio viene idrolizzato, liberando il prodotto in modo che possa diffondere fuori dal sito attivo e permettere l’inizio di un altro ciclo catalitico.
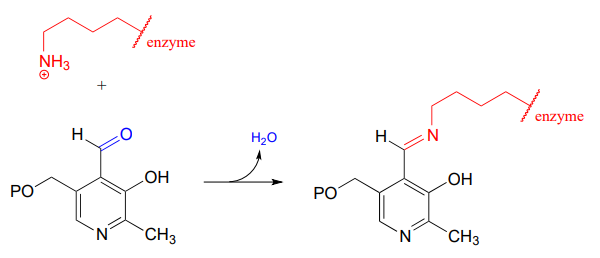
Allora, il legame imminico \(PLP\)-lisina viene scambiato con un legame imminico tra \(PLP\) e il gruppo amminico sul substrato, in quella che può essere definita una transiminazione.
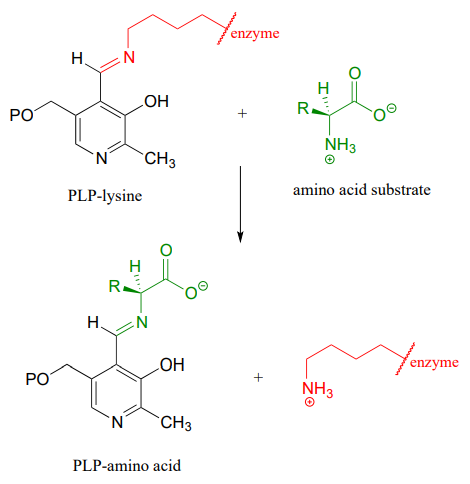
Il meccanismo di una transiminazione è molto simile a quello della formazione delle immine:
Reazione di transiminazione:
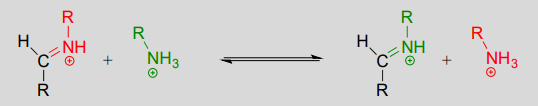
Meccanismo:
Esercizio \(\PageIndex{1})
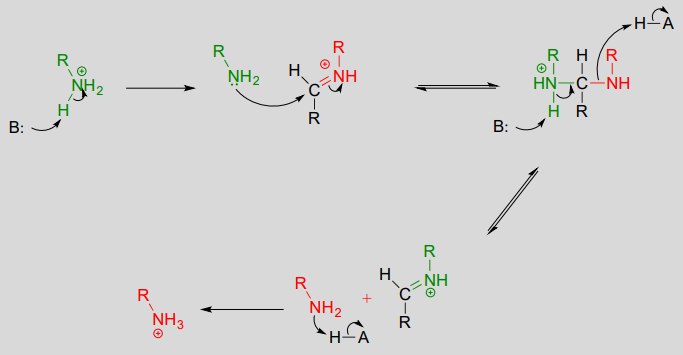
Disegna un’immina che potrebbe formarsi tra ogni coppia di composti.
a.
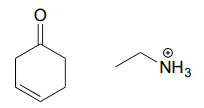
b.
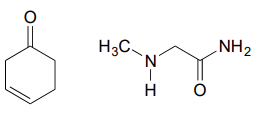
c.
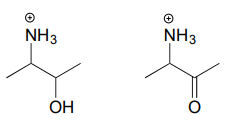
Esercizio \(\PageIndex{2})
Disegna il prodotto di idrolisi dell’imminio per ciascuno dei seguenti composti.
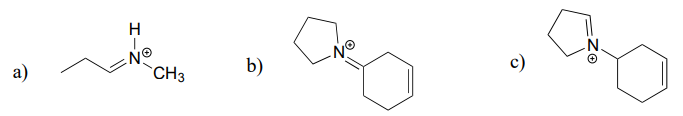
Rispondi
Aggiungi il testo della risposta qui e sarà automaticamente nascosto se hai un modello “AutoNum” attivo nella pagina.
Esercizio \(\PageIndex{3})
- L’intermedio metabolico mostrato sotto subisce una formazione intramolecolare di immina come passo nella biosintesi della lisina (EC 4.3.3.7). Disegna il prodotto di questa fase di formazione intramolecolare dell’immina.
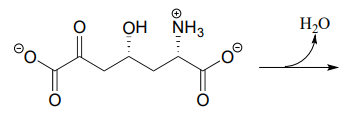
- Prevedi il prodotto di questo passo di idrolisi dell’iminio (EC 2.3.1.117) dalla via di degradazione della prolina.
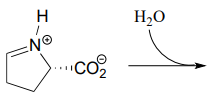
Contributori
-
Organic Chemistry With a Biological Emphasis di Tim Soderberg (University of Minnesota, Morris)