Obiettivi di apprendimento
- Apprendere i termini di base usati per descrivere la materia.
La definizione di chimica – lo studio delle interazioni della materia con altra materia e con l’energia – usa alcuni termini che dovrebbero essere definiti. Iniziamo lo studio della chimica definendo alcuni termini di base.
Materia. Un libro è materia, un computer è materia, il cibo è materia e la terra è materia. A volte la materia può essere difficile da identificare. Per esempio, l’aria è materia, ma poiché è così sottile rispetto alle altre materie (per esempio, un libro, un computer, il cibo e lo sporco), a volte dimentichiamo che l’aria ha una massa e occupa spazio. Le cose che non sono materia includono pensieri, idee, emozioni e speranze.
Esempio 1
Quale delle seguenti è materia e non materia?
- un hot dog
- l’amore
- un albero
Soluzione
- Un hot dog ha massa e occupa spazio, quindi è materia.
- L’amore è un’emozione, e le emozioni non sono materia.
- Un albero ha massa e occupa spazio, quindi è materia.
Mettiti alla prova
Quale delle seguenti è materia e non materia?
- la luna
- un’idea per una nuova invenzione
Risposta
- la luna è materia.
- L’invenzione stessa può essere materia, ma l’idea per essa non lo è.
Figura 1.1 Le fasi della materia

“Ice cubes” by Darren Hester is licensed under the Creative Commons Attribution-Share Alike 2.5 Generic; “Glass of Water” by Greg Riegler is licensed under the Creative Commons Attribution 2.0 Generic; Tea Time by Vélocia is licensed under the Creative Commons Attribution-NonCommercial- NoDerivs 2.0 Generic.
Per capire la materia e come cambia, dobbiamo essere in grado di descriverla. Ci sono due modi fondamentali per descrivere la materia: proprietà fisiche e proprietà chimiche. Le proprietà fisiche sono caratteristiche che descrivono la materia così come esiste. Alcune delle molte caratteristiche fisiche della materia sono forma, colore, dimensione e temperatura. Un’importante proprietà fisica è la fase (o stato) della materia. Le tre fasi fondamentali della materia sono il solido, il liquido e il gas (vedi Figura 1.1 “Le fasi della materia”).
Figura 1.2 Proprietà chimiche
Il fatto che questo fiammifero bruci è una proprietà chimica del fiammifero.

“acceso un fiammifero” (http://commons.wikimedia.org/wiki/File:Match_stick,_lit_a_match,_match_box,_fire.JPG) by Jith JR is licensed under the Creative Commons Attribution-Share Alike 3.0 Unported.
Le proprietà chimiche sono caratteristiche della materia che descrivono come la materia cambia forma in presenza di altra materia. Un campione di materia brucia? La combustione è una proprietà chimica. Si comporta violentemente quando viene messo in acqua? Anche questa reazione è una proprietà chimica (Figura 1.2 “Proprietà chimiche”). Nei capitoli seguenti, vedremo come le descrizioni delle proprietà fisiche e chimiche siano aspetti importanti della chimica.
Figura 1.3 Cambiamenti fisici
Il ghiaccio solido si scioglie in acqua liquida-un cambiamento fisico.

“Melting Ice Cubes” (https://www.flickr.com/photos/jariceiii/5012344135/) by Jar is licensed under Creative Commons Attribution 2.0 Generic.
Se la materia rimanesse sempre uguale, la chimica sarebbe piuttosto noiosa. Fortunatamente, una parte importante della chimica coinvolge il cambiamento. Un cambiamento fisico avviene quando un campione di materia cambia una o più delle sue proprietà fisiche. Per esempio, un solido può sciogliersi (Figura 1.3 “Cambiamenti fisici”), o l’alcol in un termometro può cambiare di volume al variare della temperatura. Un cambiamento fisico non influenza la composizione chimica della materia.
Un cambiamento chimico è il processo di dimostrazione di una proprietà chimica, come il fiammifero che brucia nella figura 1.2 “Proprietà chimiche”. Quando la materia nel fiammifero brucia, la sua composizione chimica cambia, e si creano nuove forme di materia con nuove proprietà fisiche. Nota che i cambiamenti chimici sono spesso accompagnati da cambiamenti fisici, poiché la nuova materia avrà probabilmente proprietà fisiche diverse dalla materia originale.
Esempio 2
Descrivi ogni processo come un cambiamento fisico o un cambiamento chimico.
- L’acqua nell’aria si trasforma in neve.
- I capelli di una persona vengono tagliati.
- L’impasto del pane diventa pane fresco in un forno.
Soluzione
- Perché l’acqua sta passando dalla fase gassosa alla fase solida, questo è un cambiamento fisico.
- I tuoi lunghi capelli vengono accorciati. Questo è un cambiamento fisico.
- A causa della temperatura del forno, avvengono cambiamenti chimici nell’impasto del pane per fare il pane fresco. Questi sono cambiamenti chimici. (In effetti, molta cucina comporta cambiamenti chimici.)
Test Yourself
Identifica ogni processo come un cambiamento fisico o un cambiamento chimico.
- Un fuoco sta infuriando in un camino.
- L’acqua viene riscaldata per fare una tazza di caffè.
Risposte
- cambiamento chimico
- cambiamento fisico
Un campione di materia che ha le stesse proprietà fisiche e chimiche in tutto è chiamato sostanza. A volte si usa la frase sostanza pura, ma la parola pura non è necessaria. La definizione del termine sostanza è un esempio di come la chimica abbia una definizione specifica per una parola che nel linguaggio quotidiano è usata con una definizione diversa e più vaga. Qui useremo il termine sostanza con la sua definizione strettamente chimica.
La chimica riconosce due diversi tipi di sostanze: elementi e composti. Un elemento è il tipo più semplice di sostanza chimica; non può essere scomposto in sostanze chimiche più semplici con mezzi chimici ordinari. Ci sono circa 115 elementi noti alla scienza, di cui 80 sono stabili. (Gli altri elementi sono radioattivi, una condizione che considereremo nel capitolo 15 “Chimica nucleare”). Ogni elemento ha il suo unico insieme di proprietà fisiche e chimiche. Esempi di elementi sono il ferro, il carbonio e l’oro.
Un composto è una combinazione di più di un elemento. Le proprietà fisiche e chimiche di un composto sono diverse dalle proprietà fisiche e chimiche dei suoi elementi costitutivi; cioè, si comporta come una sostanza completamente diversa. Ci sono più di 50 milioni di composti conosciuti, e altri vengono scoperti ogni giorno. Esempi di composti sono l’acqua, la penicillina e il cloruro di sodio (il nome chimico del comune sale da cucina).
Elementi e composti non sono gli unici modi in cui la materia può essere presente. Incontriamo spesso oggetti che sono combinazioni fisiche di più di un elemento o composto. Le combinazioni fisiche di più di una sostanza sono chiamate miscele. Ci sono due tipi di miscele. Un miscuglio eterogeneo è un miscuglio composto da due o più sostanze. È facile dire, a volte ad occhio nudo, che è presente più di una sostanza. Una miscela omogenea è una combinazione di due o più sostanze che è così intimamente mescolata che la miscela si comporta come una sola sostanza. Un’altra parola per una miscela omogenea è soluzione. Così, una combinazione di sale e lana d’acciaio è una miscela eterogenea perché è facile vedere quali particelle della materia sono cristalli di sale e quali sono lana d’acciaio. D’altra parte, se prendi dei cristalli di sale e li sciogli in acqua, è molto difficile dire che hai più di una sostanza presente solo guardando – anche se usi un potente microscopio. Il sale sciolto in acqua è una miscela omogenea, o una soluzione (Figura 1.4 “Tipi di miscele”).
Figura 1.4 Tipi di miscele

Esempio 3
Identificare le seguenti combinazioni come miscele eterogenee o miscele omogenee.
- acqua gassata (L’anidride carbonica è dissolta in acqua.)
- una miscela di limatura di metallo ferroso e polvere di zolfo (Sia il ferro che lo zolfo sono elementi.)
Soluzione
- Perché l’anidride carbonica è dissolta in acqua, possiamo dedurre dal comportamento dei cristalli di sale dissolti in acqua che l’anidride carbonica dissolta in acqua è (anche) una miscela omogenea.
- Assumendo che il ferro e lo zolfo siano semplicemente mescolati insieme, dovrebbe essere facile vedere cosa è ferro e cosa è zolfo, quindi questa è una miscela eterogenea.
Test Yourself
Le seguenti combinazioni sono miscele omogenee o eterogenee?
- il corpo umano
- un’amalgama, una combinazione di alcuni altri metalli dissolti in una piccola quantità di mercurio
Risposte
- miscela eterogenea
- miscela omogenea
Ci sono altri descrittori che possiamo usare per descrivere la materia, specialmente gli elementi. Di solito possiamo dividere gli elementi in metalli e non metalli, e ogni serie condivide alcune proprietà (ma non sempre tutte). Un metallo è un elemento che è solido a temperatura ambiente (anche se il mercurio è una nota eccezione), è lucido e argenteo, conduce bene l’elettricità e il calore, può essere battuto in fogli sottili (una proprietà chiamata malleabilità), e può essere tirato in fili sottili (una proprietà chiamata duttilità). Un non metallo è un elemento che è fragile quando è solido, non conduce bene l’elettricità o il calore, e non può essere trasformato in fogli sottili o fili (Figura 1.5 “Semimetalli”). I non metalli esistono anche in una varietà di fasi e colori a temperatura ambiente. Alcuni elementi hanno proprietà sia dei metalli che dei non metalli e sono chiamati semimetalli (o metalloidi). Vedremo più avanti come queste descrizioni possono essere assegnate piuttosto facilmente a vari elementi.
Figura 1.5 Semimetalli

“Pouring liquid mercury bionerd” è concesso in licenza secondo la Creative CommonsAttribution 3.0 Unported; “Sulphur-vulcano” di Heidi Soosalu è concesso in licenza secondo la Creative Commons Attribution-Share Alike 3.0 Unported.
La figura 1.6 “Descrivere la materia” è un diagramma di flusso delle relazioni tra i diversi modi di descrivere la materia.
Figura 1.6 Descrivere la materia
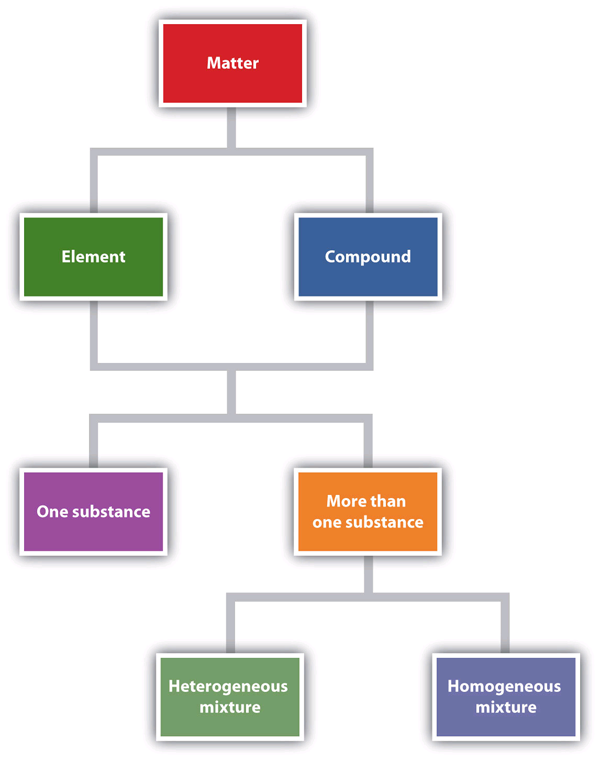
Questo diagramma di flusso mostra come la materia può essere descritta.
La chimica è ovunque: Al mattino
La maggior parte delle persone ha un rituale mattutino, un processo che compie ogni mattina per prepararsi alla giornata. La chimica appare in molte di queste attività.
- Se fai una doccia o un bagno al mattino, probabilmente usi sapone, shampoo o entrambi. Questi articoli contengono sostanze chimiche che interagiscono con l’olio e lo sporco del tuo corpo e dei tuoi capelli per rimuoverli e lavarli via. Molti di questi prodotti contengono anche sostanze chimiche che ti fanno avere un buon odore; sono chiamate fragranze.
- Quando ti lavi i denti al mattino, di solito usi il dentifricio, una forma di sapone, per pulire i denti. I dentifrici contengono tipicamente particelle minuscole e dure, chiamate abrasivi, che strofinano fisicamente i denti. Molti dentifrici contengono anche fluoruro, una sostanza che interagisce chimicamente con la superficie dei denti per aiutare a prevenire la carie.
- Forse prendi vitamine, integratori o medicine ogni mattina. Le vitamine e altri integratori contengono sostanze chimiche di cui il tuo corpo ha bisogno in piccole quantità per funzionare correttamente. Le medicine sono sostanze chimiche che aiutano a combattere le malattie e a promuovere la salute.
- Forse fai delle uova fritte per colazione. Friggere le uova comporta un riscaldamento sufficiente in modo che si verifichi una reazione chimica per cuocere le uova.
- Dopo aver mangiato, il cibo nello stomaco reagisce chimicamente in modo che il corpo (soprattutto l’intestino) possa assorbire cibo, acqua e altri nutrienti.
- Se si guida o si prende l’autobus per andare a scuola o al lavoro, si sta utilizzando un veicolo che probabilmente brucia benzina, un materiale che brucia abbastanza facilmente e fornisce energia per alimentare il veicolo. Ricorda che la combustione è un cambiamento chimico.
Questi sono solo alcuni esempi di come la chimica influenzi la tua vita quotidiana. E non siamo ancora arrivati al pranzo!
Figura 1.7 La chimica nella vita reale

“Soaps and Shampoos” by Takashi Ota is licensed under Creative Commons Attribution 2.0 Generic; “English Breakfast” è concesso in licenza secondo la Creative Commons Attribution-Share Alike 3.0 Unported; “Langley, Trans-Canada Highway” di James è concesso in licenza secondo la Creative Commons Attribution- Share Alike 3.0 Unported.

Fonte video: The chemical world by keyj (https://viuvideos.viu.ca/media/The+Chemical+World/0_ixlxmwe8)
Key Takeaways
- La chimica è lo studio della materia e delle sue interazioni con altra materia ed energia.
- La materia è tutto ciò che ha massa e occupa spazio.
- La materia può essere descritta in termini di proprietà fisiche e chimiche.
- Le proprietà fisiche e le proprietà chimiche della materia possono cambiare.
- La materia è composta da elementi e composti.
- Le combinazioni di diverse sostanze sono chiamate miscele.
- Gli elementi possono essere descritti come metalli, non metalli e semimetalli.
Esercizi
- Identifica ciascuno come materia o non materia.
a) un libro
b) odio
c) luce
d) una macchina
e) un uovo fritto
2. Fai un esempio di materia in ogni fase: solida, liquida o gassosa.
3. Ogni affermazione rappresenta una proprietà fisica o una proprietà chimica?
a) Lo zolfo è giallo.
b) La lana d’acciaio brucia se accesa da una fiamma.
c) Un gallone di latte pesa più di otto libbre.
4. Ogni affermazione rappresenta una proprietà fisica o una proprietà chimica?
a) Un mucchio di foglie marcisce lentamente in giardino.
b) In presenza di ossigeno, l’idrogeno può interagire per fare acqua.
c) L’oro può essere allungato in fili molto sottili.
5. Ogni affermazione rappresenta un cambiamento fisico o chimico?
a) L’acqua bolle e diventa vapore.
b) Il cibo viene convertito in forma utilizzabile dal sistema digestivo.
c) L’alcol in molti termometri congela a circa -40 gradi Fahrenheit.
6. Ogni affermazione rappresenta un cambiamento fisico o chimico?
a) La grafite, una forma di carbonio elementare, può essere trasformata in diamante, un’altra forma di carbonio, a temperature e pressioni molto elevate.
b) La casa di fronte è stata dipinta di un nuovo colore.
c) Gli elementi sodio e cloro si uniscono per fare una nuova sostanza chiamata cloruro di sodio.
7. Distingui tra un elemento e un composto. Quanti di ognuno sono noti?
8. Qual è la differenza tra un miscuglio omogeneo e un miscuglio eterogeneo?
9. Identificare ciascuno come un miscuglio eterogeneo o un miscuglio omogeneo.
a) Il sale si mescola con il pepe.
b) Lo zucchero si scioglie in acqua.
c) La pasta si cuoce in acqua bollente.
10. Identificare ciascuno come una miscela eterogenea o una miscela omogenea.
a) aria
b) sporcizia
c) un televisore
11. Nell’esercizio 9, quali scelte sono anche soluzioni?
12. Nell’esercizio 10, quali scelte sono anche soluzioni?
13. Perché il ferro è considerato un metallo?
14. Perché l’ossigeno è considerato un non metallo?
15. Distingui tra un metallo e un non metallo.
16. Quali proprietà hanno i semimetalli?
17. Il carbonio elementare è un solido nero dall’aspetto opaco che conduce bene il calore e l’elettricità. È molto fragile e non può essere trasformato in fogli sottili o fili lunghi. Tra queste proprietà, come si comporta il carbonio come metallo? Come si comporta il carbonio come non metallo?
18. Il silicio puro è lucido e argenteo, ma non conduce bene l’elettricità o il calore. Di queste proprietà, come si comporta il silicio come un metallo? Come si comporta il silicio come un non metallo?
Risposte
a) materia
b) non materia
c) non materia
d) materia
a) proprietà fisica
b) proprietà chimica proprietà
c) proprietà fisica
a) cambiamento fisico
b) cambiamento chimico
c) cambiamento fisico
7. Un elemento è una parte chimica fondamentale di una sostanza; ci sono circa 115 elementi conosciuti. Un composto è una combinazione di elementi che agisce come una sostanza diversa; ci sono oltre 50 milioni di sostanze conosciute.
a) eterogeneo
b) omogeneo
c) eterogeneo
11. La scelta b è una soluzione.
13. Il ferro è un metallo perché è solido, è lucido e conduce bene l’elettricità e il calore.
15. I metalli sono tipicamente lucidi, conducono bene l’elettricità e il calore e sono malleabili e duttili; i non metalli sono di vari colori e fasi, sono fragili nella fase solida e non conducono bene il calore o l’elettricità.
17. Il carbonio si comporta come un metallo perché conduce bene il calore e l’elettricità. È un non metallo perché è nero e fragile e non può essere trasformato in fogli o fili.