 Yoshinori Ohsumi
Yoshinori OhsumiNel 2016, l’Assemblea dei Nobel del Karolinska Institutet ha assegnato il Premio Nobel per la Fisiologia o la Medicina a Yoshinori Ohsumi per le sue scoperte sui meccanismi dell’autofagia.
Ma cos’è l’autofagia? La parola deriva dal greco auto (sé) e phagein (mangiare). Quindi la parola significa letteralmente mangiare se stessi. Essenzialmente, questo è il meccanismo del corpo di sbarazzarsi di tutto il macchinario cellulare vecchio e rotto (organelli, proteine e membrane cellulari) quando non c’è più abbastanza energia per sostenerlo. È un processo regolato e ordinato per degradare e riciclare i componenti cellulari.

C’è un processo simile, più noto, chiamato apoptosi, noto anche come morte cellulare programmata. Le cellule, dopo un certo numero di divisioni, sono programmate per morire. Anche se questo può sembrare un po’ macabro all’inizio, rendetevi conto che questo processo è essenziale per mantenere una buona salute. Per esempio, supponiamo che tu possieda una macchina. Amate questa macchina. Avete grandi ricordi in essa. Ma dopo qualche anno, inizia a sembrare un po’ malconcia. Dopo alcuni altri, non sembra così grande. L’auto ti costa migliaia di dollari ogni anno per la manutenzione. Si rompe continuamente. È meglio tenerla in giro quando non è altro che un rottame? Ovviamente no. Così te ne sbarazzi e compri un’auto nuova di zecca.
La stessa cosa accade nel corpo. Le cellule diventano vecchie e malandate. È meglio che siano programmate per morire quando la loro vita utile è finita. Sembra davvero crudele, ma questa è la vita. Questo è il processo di apoptosi, dove le cellule sono predestinate a morire dopo un certo periodo di tempo. È come affittare una macchina. Dopo un certo periodo di tempo, ti sbarazzi dell’auto, che sia ancora funzionante o meno. Poi prendi una nuova macchina. Non devi preoccuparti che si rompa nel momento peggiore possibile.
Autofagia – sostituire le vecchie parti della cellula
Lo stesso processo avviene anche a livello sub-cellulare. Non c’è necessariamente bisogno di sostituire l’intera macchina. A volte basta sostituire la batteria, buttare via quella vecchia e prenderne una nuova. Questo succede anche nelle cellule. Invece di uccidere l’intera cellula (apoptosi), si vuole sostituire solo alcune parti della cellula. Questo è il processo di autofagia, dove gli organelli subcellulari vengono distrutti e ne vengono ricostruiti di nuovi per sostituirli. Le vecchie membrane cellulari, gli organelli e altri detriti cellulari possono essere rimossi. Questo viene fatto inviandoli al lisosoma che è un organello specializzato che contiene enzimi per degradare le proteine.
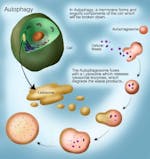
L’autofagia fu descritta per la prima volta nel 1962 quando i ricercatori notarono un aumento del numero di lisosomi (la parte della cellula che distrugge le cose) nelle cellule del fegato di ratto dopo aver infuso glucagone. Il premio Nobel Christian de Duve ha coniato il termine autofagia. Le parti subcellulari danneggiate e le proteine inutilizzate vengono contrassegnate per la distruzione e poi inviate ai lisosomi per finire il lavoro.
Uno dei regolatori chiave dell’autofagia è la chinasi chiamata mammalian target of rapamycin (mTOR). Quando mTOR è attivato, sopprime l’autofagia, e quando è inattivo, la promuove.
Cosa attiva l’autofagia?
La privazione di nutrienti è l’attivatore chiave dell’autofagia. Ricordate che il glucagone è una specie di ormone opposto all’insulina. È come il gioco che facevamo da bambini – ‘giorno opposto’. Se l’insulina sale, il glucagone scende. Se l’insulina scende, il glucagone sale. Quando mangiamo, l’insulina sale e il glucagone scende. Quando non mangiamo (digiuno) l’insulina va giù e il glucagone va su. Questo aumento del glucagone stimola il processo di autofagia. In effetti, il digiuno (aumenta il glucagone) fornisce la più grande spinta conosciuta all’autofagia.
Il digiuno è in realtà molto più benefico che stimolare semplicemente l’autofagia. Fa due cose buone. Stimolando l’autofagia, stiamo eliminando tutte le nostre vecchie proteine e parti cellulari. Allo stesso tempo, il digiuno stimola anche l’ormone della crescita, che dice al nostro corpo di iniziare a produrre nuove parti per il corpo. Stiamo davvero dando al nostro corpo il rinnovamento completo.
È necessario sbarazzarsi della roba vecchia prima di poter mettere roba nuova. Pensate a rinnovare la vostra cucina. Se avete dei vecchi armadietti verde lime stile anni ’70 in giro, dovete buttarli via prima di metterne di nuovi. Quindi il processo di distruzione (rimozione) è importante quanto il processo di creazione. Se si cercasse semplicemente di mettere nuovi armadi senza togliere quelli vecchi, non sarebbe così bello. Così il digiuno può in qualche modo invertire il processo di invecchiamento, liberandosi della vecchia spazzatura cellulare e sostituendola con parti nuove.
Un processo altamente controllato
L’autofagia è un processo altamente regolato. Se si scatena, fuori controllo, sarebbe dannoso, quindi deve essere attentamente controllato. Nelle cellule di mammifero, l’esaurimento totale degli aminoacidi è un forte segnale per l’autofagia, ma il ruolo dei singoli aminoacidi è più variabile. Tuttavia, i livelli plasmatici di aminoacidi variano solo di poco. Si pensa che i segnali degli aminoacidi e quelli del fattore di crescita/insulina convergano sulla via mTOR – a volte chiamata il regolatore principale della segnalazione dei nutrienti.
Quindi, durante l’autofagia, i vecchi componenti delle cellule vengono scomposti negli aminoacidi componenti (il blocco di costruzione delle proteine). Cosa succede a questi aminoacidi? Nelle prime fasi della fame, i livelli di aminoacidi iniziano ad aumentare. Si pensa che questi aminoacidi derivati dall’autofagia siano consegnati al fegato per la gluconeogenesi. Possono anche essere scomposti in glucosio attraverso il ciclo dell’acido tricarbossilico (TCA). Il terzo potenziale destino degli aminoacidi è quello di essere incorporati in nuove proteine.
Le conseguenze dell’accumulo di vecchie proteine spazzatura dappertutto possono essere viste in due condizioni principali – il morbo di Alzheimer (AD) e il cancro. Il morbo di Alzheimer comporta l’accumulo di proteine anormali, sia la beta amiloide che la proteina Tau, che incasina il sistema cerebrale. Anche se non abbiamo ancora prove cliniche per questo, avrebbe senso che un processo come l’autofagia che ha la capacità di eliminare le vecchie proteine potrebbe prevenire lo sviluppo dell’AD.
Cosa spegne l’autofagia? Mangiare. Il glucosio, l’insulina (o la diminuzione del glucagone) e le proteine spengono questo processo di autopulizia. E non ci vuole molto. Anche una piccola quantità di aminoacido (leucina) potrebbe fermare l’autofagia a freddo. Quindi questo processo di autofagia è unico nel digiuno – qualcosa che non si trova nella semplice restrizione calorica o nella dieta.
C’è un equilibrio qui, naturalmente. Ci si ammala sia per troppa autofagia che per troppo poca. Il che ci riporta al ciclo naturale della vita: festa e digiuno. Non una dieta costante. Questo permette la crescita cellulare durante il consumo e la pulizia cellulare durante il digiuno – l’equilibrio. La vita è tutta una questione di equilibrio.
–
Jason Fung