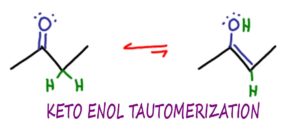
 Keto Enol Tautomerization o KET, è una reazione di chimica organica in cui le molecole di chetone ed enolo possono isomerizzare o interconvertirsi, tipicamente in una reazione catalizzata da acido o base.
Keto Enol Tautomerization o KET, è una reazione di chimica organica in cui le molecole di chetone ed enolo possono isomerizzare o interconvertirsi, tipicamente in una reazione catalizzata da acido o base.
La tautomerizzazione cheto-enolo si presenterà un bel po’ di volte nel tuo corso di chimica organica, iniziando con le reazioni di idratazione degli alcheni, e spuntando di nuovo nelle tue reazioni avanzate (orgo 2) di enolato e condensazione.
La tautomerizzazione è un tipo molto specifico di isomerizzazione,
in questo caso l’interconversione tra le forme cheto ed enolo di una molecola.

Keto si riferisce al gruppo funzionale chetonico – anche se il KET non è limitato ai chetoni JUST.
Anche le aldeidi, che sono molto simili ai chetoni,
tranne che per un idrogeno terminale,
possono subire la tautomerizzazione.
 Enolo deriva da ‘Ene’ come in alchene,
Enolo deriva da ‘Ene’ come in alchene,
un doppio legame carbonio-carbonio.
E ‘ol’ come in alcol – un gruppo OH.
Ti senti arrugginito? Ripassa i gruppi funzionali della chimica organica
Se la tautomerizzazione è come l’isomerizzazione,
Pensa ai tautomeri come agli isomeri, in particolare agli isomeri costituzionali.
Il termine tautomeri si riferisce alle due forme specifiche della molecola che possono interconvertirsi all’equilibrio.
Nel KET, le forme cheto ed enolo sono tautomeri l’una dell’altra.

Qual è più stabile, cheto o enolo?
Nonostante sia una reazione reversibile, la forma cheto è più stabile e quindi favorita dall’equilibrio.
Questo perché il carbonio doppio legato all’ossigeno è più stabile del carbonio singolo legato all’ossigeno e del carbonio singolo legato all’idrogeno.
Per fortuna, questa matematica viene dalla termodinamica trattata in chimica generale e qualcosa che non devi calcolare a livello di chimica organica (alcuni professori lo richiedono ancora però).
Questa non è una regola dura e veloce.
Ci sono alcune situazioni in cui la forma enol darà maggiore stabilità alla molecola complessiva. Date un’occhiata all’esempio qui sotto:

La forma cheto ha un carbonile più stabile, ma la forma enol permette al legame pi di essere parte di un sistema aromatico molto più stabile (rivedere l’aromaticità qui). Pertanto, la forma enol di questa molecola predominerà all’equilibrio.
La tautomerizzazione cheto- enol si presenta in varie reazioni organiche, a partire dall’idroborazione e dall’ossimercurazione degli alchini.
KET nell’ossimercurazione degli alchini
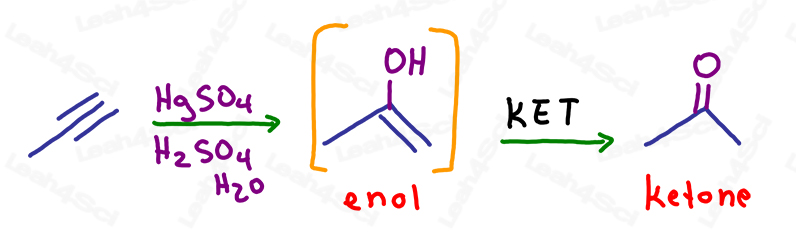
Come per gli alcheni, la reazione di ossimercurazione rompe semplicemente UN legame pi greco per aggiungere un alcol al carbonio più sostituito, seguendo la regola di Markovnikov.
La molecola risultante ha ancora un legame pi: un alchene sullo stesso carbonio dell’alcool.
Questo è un enolo instabile e subirà automaticamente la tautomerizzazione del cheto enolo per formare un prodotto finale chetone più stabile.
KET nell’idroborazione degli alchini
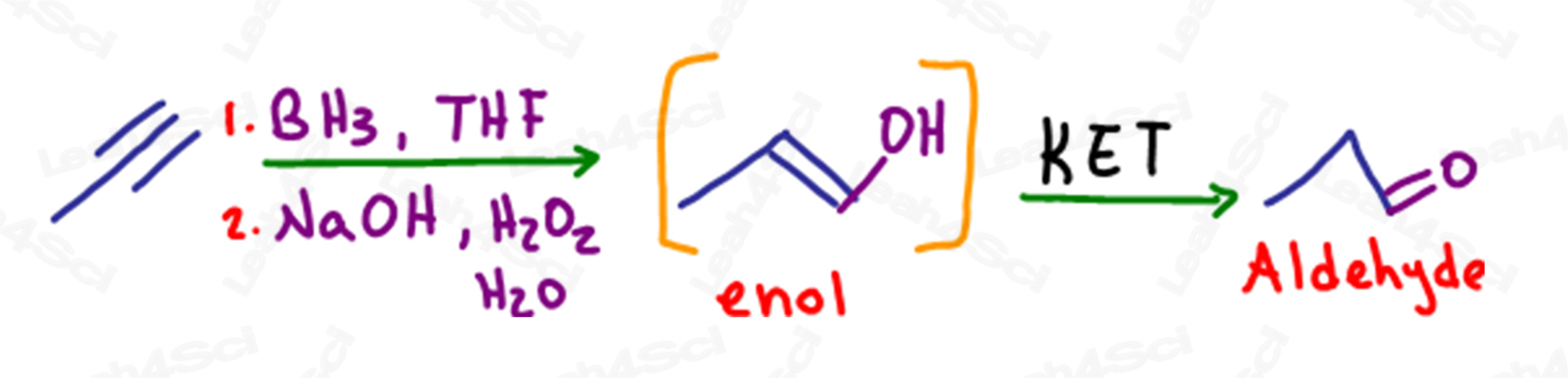
Come per gli alcheni, l’idroborazione è una reazione anti-Markovnikov in cui un legame pi è rotto e un alcol è aggiunto al carbonio meno sostituito.
Nel caso di un alchene terminale, quando un singolo legame pi è trasformato in un alcool, il carbonio terminale ha ancora un legame pi o un alchene, rendendolo un enolo.
Questa molecola subirà anche una tautomerizzazione per formare un prodotto aldeide più stabile.
Anche se forma un’aldeide, questa reazione è ancora considerata una tautomerizzazione cheto enolica.
Per queste 2 reazioni, il chetone o l’aldeide risultante è determinato dalla posizione dell’enolo.
Se l’enolo è su un carbonio interno (non terminale), il prodotto risultante formerà un chetone.
Se l’enolo è terminale, allora il carbonile risultante sarà un’aldeide.
La tautomerizzazione può avvenire sia in condizioni catalizzate da acido che da base.
Con le reazioni di cui sopra, considera quali devono essere le condizioni dopo aver subito l’idratazione come scritto.
Il video qui sotto vi guida passo dopo passo
- Reazione di tautomerizzazione catalizzata da acido e meccanismo
- Reazione di tautomerizzazione catalizzata da base e meccanismo
- La reazione inversa (da cheto a enolo) per entrambe le reazioni
Tautomerizzazione catalizzata da acidoMeccanismo di tautomerizzazione catalizzata
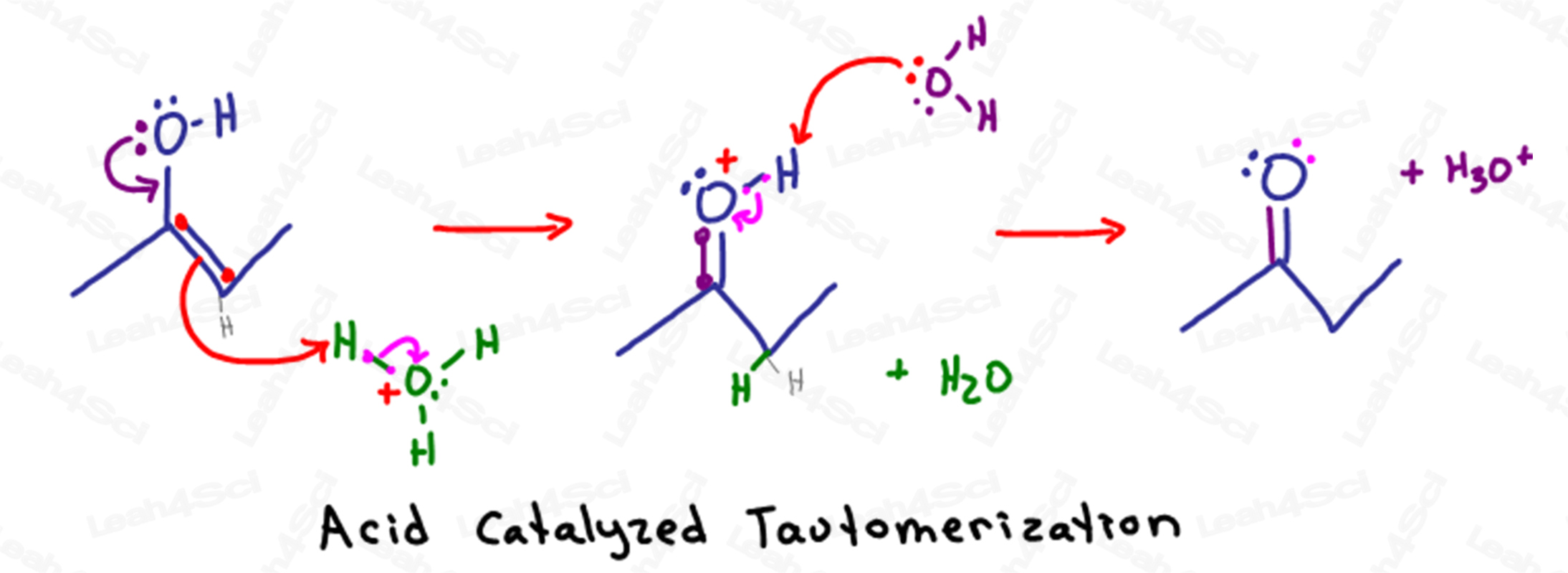
Ricordo che nelle soluzioni acquose acide abbiamo molta acqua e idronio (H3O+) disponibili in soluzione.
La tautomerizzazione inizia quando gli elettroni parzialmente negativi dell’ossigeno dell’alcool scendono ad attaccare l’atomo di carbonio sp2 (quello che tiene il legame pi).
Formando un secondo legame tra carbonio e ossigeno, il carbonio avrebbe un totale di 5 legami.
Per evitare di violare il suo ottetto, il carbonio butta fuori il legame pi tra se stesso e l’altro atomo di carbonio sp2 spingendo gli elettroni sull’altro carbonio.
Invece di stare come coppia solitaria sul carbonio, gli elettroni negativi sono attratti dall’atomo parzialmente positivo H+ su una molecola di idronio vicina.
Poiché quell’atomo H+ può avere solo un legame, lascia andare gli elettroni che lo tengono legato all’ossigeno, permettendo all’acqua di galleggiare via in soluzione.
La molecola risultante sembra un chetone, tranne che per l’atomo instabile di ossigeno.
L’ossigeno, con 2 legami al carbonio, 1 legame all’idrogeno, e una singola coppia solitaria, ha una carica positiva instabile.
Un’altra molecola d’acqua in soluzione usa i suoi elettroni parzialmente negativi per deprotonare l’ossigeno e restituire così i suoi elettroni per formare un chetone neutro stabile.
Facciamo un po’ di conti veloci.
Questa reazione è iniziata quando l’enolo ha attaccato l’idronio, il nostro catalizzatore acido.
Nella fase finale, l’acqua deprotonifica il chetone, riformando il nostro catalizzatore acido idronio.
Ricordo: se l’enolo è terminale il prodotto risultante è un’aldeide invece di un chetone
Meccanismo di tautomerizzazione catalizzata da basi
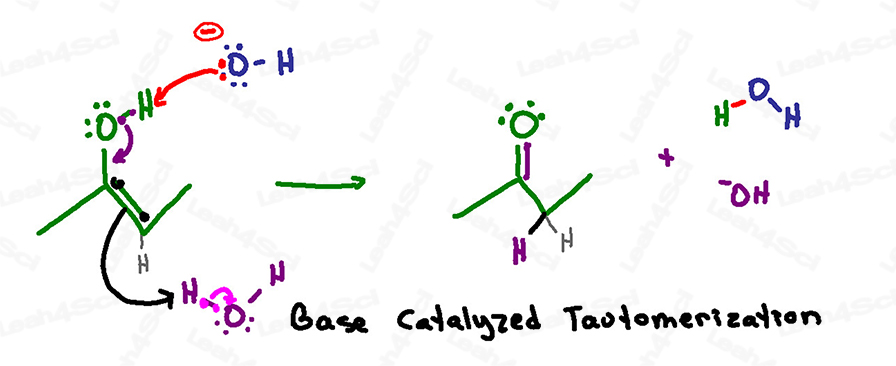
Ricordo: in una soluzione acquosa basica abbiamo sia idrossido che acqua che galleggiano intorno.
Non mostrare mai H+ o idronio in una soluzione basica!
Questa reazione è molto simile al meccanismo catalizzato dall’acido, tranne che la deprotonazione è il primo passo piuttosto che quello finale.
Questo perché la soluzione basica può gestire un ossigeno negativo, ma la soluzione acida non permette la formazione di un ossigeno negativo.
Questa reazione inizia quando un idrossido basico in soluzione raggiunge l’idrogeno acido sull’enolo.
Invece di collassare di nuovo sull’ossigeno per formare un ossido negativo, gli elettroni collassano rapidamente verso il basso per formare un legame pi carbonile tra carbonio e ossigeno.
Come nel meccanismo catalizzato dall’acido, il carbonio deve cacciare il suo doppio legame attuale per evitare di avere 5 legami e violare il suo ottetto.
Gli elettroni del legame pi non si siedono e aspettano sull’altro carbonio, invece, cercano e prendono un protone dalla soluzione – prendendolo da una molecola d’acqua.
In una singola serie di attacchi (un passo), abbiamo un chetone come prodotto finale.
Fate attenzione a cosa è stato usato e riformato in questa reazione:
L’idrossido ha afferrato un protone formando acqua,
ma l’enolo ha afferrato un protone dall’acqua formando idrossido e riformando così il catalizzatore di base che ha iniziato questa reazione.
Ricordo: se l’enolo è terminale il prodotto risultante è un aldeide invece di un chetone