はじめに
ヒト乳頭腫ウイルス(HPV)は、ヘリコイド状の二本鎖DNA分子とタンパク質のカプシドで構成されている異質なウイルスグループです。 HPVは、上皮の基底状態に感染し、その結果、DNAの転写と複製を基底レベルで維持し、皮膚や粘膜に過形成の乳頭状および疣状の病変を形成する上皮向性物質で構成されています1
HPVには230種類以上の型があり(うち118種類はよく知られています)、40種類以上の肛門性器型があり、そのうち15種類は発癌性があります。 2,3
舌のHPVの場合、臨床症状には大きく分けて2つのグループがあります:
a)良性病変、b)前悪性病変または悪性病変。 良性病変としては、口腔乳頭腫、尋常性口腔疣贅(尋常性疣贅)、コンジローマ、巣状上皮過形成(ヘックス病)などが挙げられます4-6。悪性および前悪性病変としては、主に白板症や扁平上皮癌が挙げられます7。
口腔粘膜の扁平上皮乳頭腫は、最も頻繁に見られる乳頭状病変で、口腔内に見られる病変全体の2.5%を占めています6。HPVの臨床病変は、上唇、下唇、舌小帯、舌背、口角に最も頻繁に見られます8。
これらの病変の最も一般的な形態は、カリフラワーのような形をしていますが、一般的なイボや角質増殖、あるいは表面的な色の変化(通常は紫色の色調)を示す非角質化表面など、他の形状も観察されます。
本研究の目的は、口腔乳頭腫症のレビューに関する文献調査を行うとともに、臨床例を報告することです。
HISTOLOGY OF THE TONGUE
舌に存在する細胞は、多元的な構造配列をしています。
舌に存在する細胞は、角質層(表層)、顆粒層、有棘層、基底層(最深層)の順に配置されている。 11
ウイルス粒子は、95%のタンパク質L1と5%のタンパク質L2からなるタンパク質カプシドで構成されている。 これらのタンパク質は連結して正20面体のカプソマーを形成する。 カプシドの内部には、約8000塩基対の二本鎖の円形DNAが存在する。 カプシドは、8つの遺伝子と非コード化された制御領域によって形成されています。この領域には、ウイルスが複製サイクルを完了するために必要な、宿主のホルモンやタンパク質因子の連結部位が含まれています。 E1、E2、E4、E5、E6、E7(E4は後期遺伝子とされている)、および2つの後期遺伝子、L1とL2である。 初期遺伝子は、ウイルスの複製や制御、発がん性に関わるタンパク質をコード化している。
HPVは、舌の上皮にできた小さな擦り傷から宿主に侵入します。
感染した細胞が分化し、基底層から上皮の有棘層に移動すると(免疫学的に許容される)、ウイルスの複製が刺激され、核内にビリオンが蓄積し、細胞質内でキャプシドが形成されます。
溶血性感染の場合、ウイルスは複製能力を持ってパラ基底細胞に到達し、細胞質を経て核に侵入します。 核に侵入したウイルスは、細胞のゲノムに組み込まれることなくエピソーム領域で複製を行い、約20のウイルスコピーを生成する。
溶血性感染の場合、細胞ゲノムは直接影響を受けます。 これはハイリスクHPV(16と18)の場合です。 細胞核に到達したウイルスは、宿主の細胞ゲノム、主にセグメントE6とE7に統合されます。 この場合、ウイルスの複製は、宿主細胞が自身のDNAと統合されたウイルスのDNAを複製するまで、潜伏期に入ります。
異なるHPVタイプの遺伝子発現は、AP-1、ケラチノサイト特異的因子、NF-1CTF、CEFI、CEFII、TEFIなどの転写因子やホルモン由来の因子によって厳密かつ特異的に制御されています。
どちらのタイプの感染症でも、E1とE2タンパク質は上昇方向に発現を開始し(supraregulation)、基底細胞の制御された発現と同様にDNA転写を活性化します12。
E6とE7 HPVの遺伝子は、E6とE7という腫瘍タンパク質を介して、細胞の悪性化に直接関係しています。 これらのタンパク質は、細胞周期を制御する細胞の遺伝子産物と化合物を形成することができ、その中にはp53とRbが含まれます。
Rbタンパク質はG1からSへの移行を制御しています。オンコプロテインE7はRbを封じ込め、Rbが細胞増殖タンパク質を制御できないようにすることで、細胞周期を合成期に留めることができます。
タンパク質E2、E3、E4、E5、E6、E7は、遺伝子のタンパク質制御を失い(核中心部にエピソームDNA)、E6とE7はウイルスDNAを複製します。
舌乳頭腫などの良性病変では、エピソーマルDNA粒子の増殖が上皮の異常増殖を促し、細胞の遺伝子エラーを増加させる(胃原性)
E6とE7はウイルスの増殖と不死化を促進する。
E6とE7は、ウイルスの増殖と不死化を促進します。ウイルスに発がん性がある場合は悪性化し、ない場合は良性の病変が形成され、2年間で自己限定することができます。 このメカニズムは、主にDNAのテロメアの消失によって引き起こされ、アポトーシスが阻害され、感染細胞数が増加し、p53やRbのアセチル化やリン酸化が減少する。 さらに、血管新生因子の発現が促進される。 例えば、血管成長因子は、細胞の細胞骨格や細胞外マトリックスを乱し、これらの構造の健全性に関与する調節因子に影響を与えます12。
HPVに感染すると、細胞の形態に重要な変化が起こります。例えば、核周囲の空胞形成、核の拡大、不規則で高色素性の核、二重核化などが観察されます。
軟骨腫は、HPV感染の最も一般的な形態学的症状です(尖圭コンジローマ)。 彼女は家の外では働いておらず、Estado de Mexico(メキシコ州)で生まれ、住んでいました。 血液型はO型で、Rh陽性でした。 家族歴としては、父親が多発性硬化症、姉が関節リウマチであることを報告していました。 患者は薬物中毒を否定した。 左乳房に多発性の若年性乳房線維腺腫があり、手術で治療しました。 15歳で初潮を迎え、月経リズムは28×3、性行為は17歳で始まった。 性的に活発なパートナーは1人で、オーラル・ジェニタル・セックスを否定していた。
その1年前に、彼女は乳房検診に加えて、下性器の細胞診とコルポスコピー検査を受けていました。 その結果、癌とHPVは陰性でした。
患者は2014年4月に初めて診察を受け、3ヶ月間の経過で腹側の舌痛症を訴えました。 その後、軟部組織に異物感と膨らみを感じ、遠心成長が進み、硬口蓋への接触時や咀嚼時に出血するレンズ状の腫瘍が形成されたとのこと。
口腔内を0.66倍に拡大したコルポスコピー(Hinselmann社製コルポスコープ、2014年メキシコ)で検査しました。 その結果、直径約1cm、ピンクがかった色、円形、ギザギザのエッジ、ペディクルなし、無血管性の病変が発見されました(図1)。
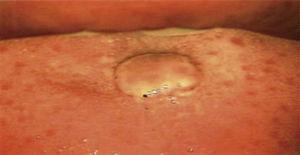
コルポスコープの視点で口内を直視したもの。 I(Hinselmann, 2014)、0.66の倍率で。 直径1cmの病変、ピンクがかった色調、円形、ギザギザのエッジ、無血管、ペディクルなし
TREATMENT
局所麻酔下、エピネフリン入り2%キシロカイン(1mL)を30G口径の針で病変部の基部に浸潤させた。 病変部の表面を切り取り、くさび型の鋭利な解剖を行いました。 止血後、境界部をDermalon 000を用いて一平面に反転縫合した。
15日後に抜糸し、健康な手術部位を得ました(図2)。 病理検査の結果、0.6×0.5cmの大きさの組織が見つかりました。 組織は不定形で,暗褐色を呈しており,軟らかかった。 顕微鏡で観察すると,多層化した角膜上皮,有棘細胞,角化亢進が認められた。 試料の内部には大きさの異なる上皮内角化病巣が認められた。 一般に、上皮細胞は正常な有棘層のものよりも小さいサイズであった(図3、4)。 最終的には舌の扁平上皮乳頭腫と診断された。
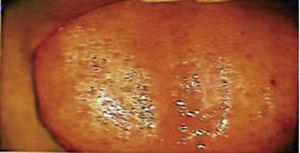
Photograph of the tongue under colposcopic perspective after 15 days after the surgery.
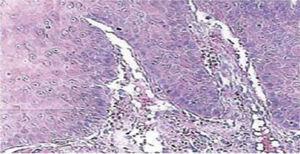
10倍の顕微鏡拡大図。 多層化した角質上皮、有棘化と角質肥厚.
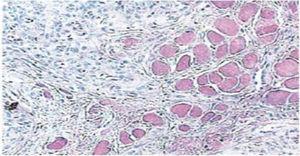
40 x Microscopic enlargement(顕微鏡拡大)。
DISCUSSION
HPVはDNAウイルスであり、パピローマウイルス科に属しています。 230以上の遺伝子型が報告されています。 潜伏期間は3週間から8ヶ月で、平均3ヶ月です。 230種類のパピローマウイルスの遺伝子型のうち、16種類が最も頻繁に口腔内病変と関連しています(1、2、3、4、6、7、10、11、13、16、31、32、33、35、57)。
HPVの臨床症状には、a)良性病変とb)前悪性または悪性病変の2つの主なグループがあります。 口腔内良性病変としては、口腔乳頭腫、尋常性疣贅(一般的なイボ)、口腔尖圭コンジローマ、巣状上皮過形成(ヘック病)などが挙げられます。 前悪性および悪性の病変は、主に遺伝子型16および18に関連する白板症および扁平上皮癌に代表されます。
HPVの診断にはいくつかの方法があり、従来の細胞診、液体ベースの細胞診、組織診、コルポスコピー、in situ hybridationやポリメラーゼ連鎖反応(PCR)などの分子生物学的手法が挙げられます15,16。
治療は個々の症例に合わせて行われます。
治療は個々の症例に合わせて行われ、凍結療法や電気手術、免疫調整剤(イミキモド5%)の使用、RNA(リボ核酸)やDNAを阻害する代謝拮抗剤の使用、チミジル酸合成酵素の阻害(5-フルオロラシル)などの破壊的手法が用いられる。
微小な外傷にさらされた口腔粘膜では、微生物や化学的・物理的要因がHPVと相乗的に作用して、良性病変や癌の発生を促すことがあります。
HPVは、肛門や生殖器、疣状表皮発育症、喉頭などの扁平上皮癌の発生に重要な役割を果たしています。
良性の病変では、遺伝子型は33と32が多いのですが、私たちの研究では、分子生物学的手法により遺伝子型58の存在が報告されています。
この疾患にうまくアプローチするためには、コルポスコープの観点からこれらの病変の研究に適した訓練を受けた歯科医、腫瘍医、婦人科医による学際的な診断と治療が最も重要です。
病変のない境界線を残すことを目的とした冷たいメスを使った外科的介入による治療は、この種の病変を根絶し、後遺症を残さないための適切な解決策であり、特に臨床的には良性のように見えるが、遺伝子タイプによっては中長期的には悪性の挙動を示す腫瘍の場合には有効である。