Pravin U. Dugel, MD
Phoenix
Pseudophakic cystoid macular edemaは、1953年にA.Ray Irvine Jr.MD,1によって最初に記述され、1969年にJ.Donald M Gass MDによってさらに解明されました。 Gass博士は、発症のピークが術後6週間であることを述べ、少数の患者が視力低下を訴えているという点で、血管造影上のPCMEと臨床的に有意なPCMEには違いがあることを示唆しました。 現在、臨床的なPCMEは、スレン視力が20/40以下と定義されています。
カプセル外白内障摘出術に代わって超音波乳化術が採用されたことで、PCMEの発生率は16~24%の範囲から低下しましたが3、多焦点眼内レンズインプラントの使用が増えたことで、患者の期待が高まっています。 多焦点眼内レンズは、もともとコントラスト感度が低下するように設計されているため、軽度のPCMEであっても、視力の質や患者の満足度を著しく低下させてしまいます。 米国食品医薬品局(FDA)は、新しい眼内レンズの使用を承認する際に、臨床的に重要なPCMEの「許容可能な割合」を5%未満にすべきだとしています。
発生率
合併症のない低リスクの患者における超音波乳化術後のPCMEの発生率は、2%から12%と幅があります4,5。 この集団におけるPCME発症の予測因子としては、網膜静脈閉塞症の既往、網膜上膜の存在、術前のプロスタグランジンの使用などが挙げられます4。 Heier JS, et al.Phacoemulsification後にCMEを発症した患者の特徴。 (Heier JS, et al. Annual Meeting of the American Academy of Ophthalmology; November 2007; New Orleans, LA.にて発表。)
Mechanism
PCMEが発症するメカニズムは、様々な程度の炎症的および機械的要素を持つ多因子性のものである。 前眼部を手術すると、細胞膜からアラカドン酸が放出され、シクロオキシゲナーゼ(COX)経路でプロスタグランジンが、リポキシゲナーゼ(LOX)経路でロイコトリエンが産生されます(図1参照)。
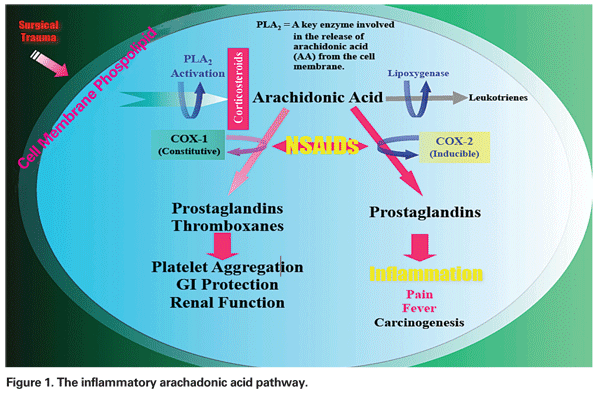
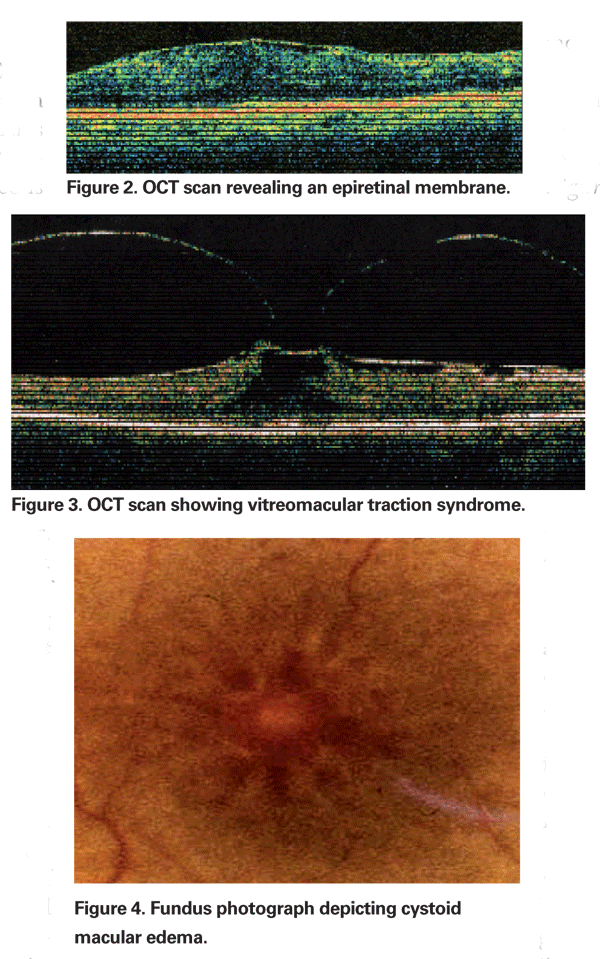
時には、白内障の摘出によって生じた炎症が後ヒアリン骨面の収縮を引き起こし、傍小窩の毛細血管の歪みとその結果としての黄斑浮腫を引き起こすことがあります。 PCMEの評価には、光干渉断層計の使用が増えてきています。 OCT画像は、硝子体黄斑牽引や網膜上膜など、CMEの機械的要素を特定するのに役立ちます(図2 & 3参照)。
他の同定可能な病因を持たない低リスク患者の慢性難治性PCMEの稀なケースでは、水晶体の破片の保持、IOLの位置異常、またはPropionibacterium acnesの感染の有無を注意深く観察しなければなりません。
診断
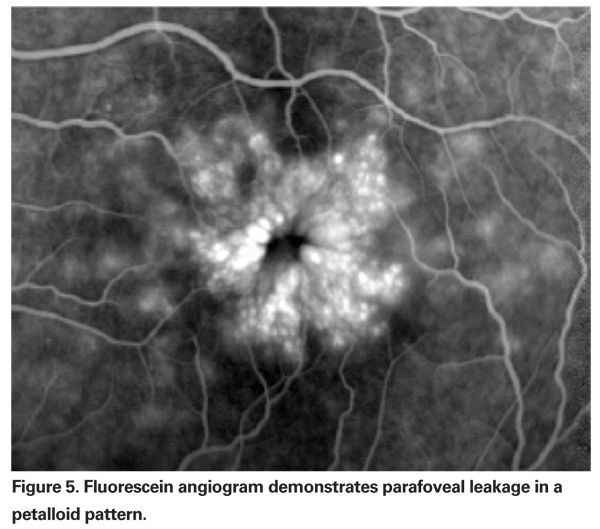
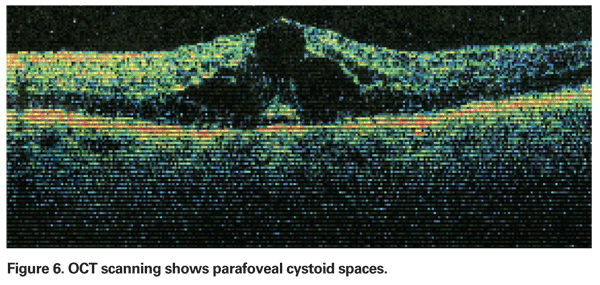
PCMEは、他の病因が認められない場合に疑うべきである。 基礎的な危険因子を持たない患者が、白内障摘出後に視力低下や変視症を訴えた場合、PCMEを疑うべきである。 臨床的には、網膜内に浮腫があり、それが蜂の巣状に広がっているのが見えます(図4参照)。 フルオレセインアンギオグラムでは、視床下部の網膜内腔にペタロイド状の漏れが見られ、視床下部の蛍光増白も見られる(図5参照)。 OCTでは、これらの嚢胞状の空間を明確に示すとともに、黄斑中心部の厚さや黄斑の総体積を算出することができます(図6参照)。 OCTの利点は、高感度、非侵襲性、解剖学的情報の提供、黄斑浮腫の定量化などですが、これらの値と視機能との相関には疑問があります。
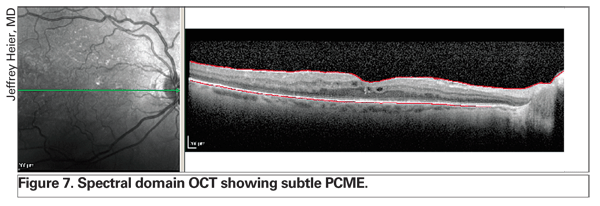
OCTの使用は、網膜浮腫の管理に革命をもたらしています。 スペクトルドメインOCTを含む新しい技術は、より優れた解像度を提供し、細隙灯生体顕微鏡やフルオレセイン血管造影よりも早く微妙なPCMEを検出できる可能性があります(図7参照)。 さらに、この改良された機器により、臨床医は、専ら網膜内の浮腫と、網膜下または色素上皮下の液体とを区別することができ、これにより予後に関する情報が得られる可能性があります(図8参照)。 網膜下色素上皮剥離があると、予後が悪くなる可能性があるというのが、複数の網膜専門医の経験である。
予防
予防的な非ステロイド性抗炎症薬の効果を評価したレトロスペクティブレビューやプロスペクティブトライアルがいくつかあります。非ステロイド性抗炎症薬を術前に使用した場合と術後に使用した場合のPCME発生率に対する効果を評価したレトロスペクティブレビューやプロスペクティブトライアルがいくつかある。 また、別のグループでは、術前にジクロフェナクナトリウム(ボルタレン)を2日間投与し、術後にジクロフェナクとコルチコステロイドの併用療法を行うことで、術後のコルチコステロイド単独療法と比較して、PCMEが12%から0%に減少したと報告しています5。
OCTを用いて黄斑部の体積を定量化した結果、術前にケトロラックを2日間投与し、術後にケトロラック/ステロイドを用いた併用療法を行うことで、ステロイドのみの対照群と比較して、術後1カ月の黄斑部の腫れが46%減少したことがわかりました7。 最近、術前に3日間のケトロラックと併用療法を行う群と、副腎皮質ステロイド単独群を比較した無作為化前向き試験では、OCTに基づいて、対照群の患者のPCME発生率が2.4%であったのに対し、併用群では0%であったことが報告されました8。 副腎皮質ステロイド群の患者は、15μm以上の網膜肥厚の発生率が有意に高かったものの、術後4週間後の最高矯正視力には両群間で統計的な差はありませんでした。
術前にインドメタシンを3日間局所投与した後に併用療法を行う群、術後に併用療法のみを行う群、コルチコステロイドのみを行う群の3群に分けて前向きに評価したところ、血管造影上のPCMEの発生率が32.8%(コルチコステロイドのみ)→15%(術後併用)→0%(術前・術後NSAID)となりました。9
また、術後のコルチコステロイドレジメンにネパフェナクナトリウム(ネバナック)を追加することで、コルチコステロイドのみの場合と比較して、PCMEの発生率が2.1%から0%に減少したという報告もあります10。 術後にジクロフェナク単独とベタメタゾンを比較した最近のプロスペクティブ・ランダマイズ比較では、術後5週間の時点で、血管造影CMEの発生率はNSAID群(18.8%)がコルチコステロイド群(58.0%)よりも低いことがわかりました。11
これらの研究は、NSAIDの予防的使用がPCMEの発生率を低下させることを示しており、その効果は少なくとも術前3日に開始し、術後数週間継続することで最大となることを示しています。 しかし、術前および術後の治療の正確なタイミングと期間、そして最も効果的な患者の特定については、まだ明らかにされていません。
ハイリスクの特徴
前述したように、1.659例の連続した症例では、エピレイトは1,659件の連続した症例では、網膜上膜、静脈閉塞の既往、プロスタグランジンアナログの術前使用がPCME発症のリスクを大きく高めていました。4 別のグループは、PCMEの管理のために網膜クリニックに紹介された連続した患者を調査したところ、糖尿病、高血圧、眼の手術の経験、網膜上膜、複雑な白内障の摘出が高リスクの特徴であることを発見しました。 Heier JS, et al.)様々な内科的疾患や眼疾患がPCME発症の素因となっていることを考えると、これらの患者を特定し、NSAID外用薬による積極的な予防的治療を行うことで、PCME発症のリスクを軽減する必要があります。
治療法
– NSAIDs。 このクラスの薬は、COX経路の阻害を介してプロスタグランジンの産生を抑制します(図1参照)。 NSAIDは、プロスタグランジンの生成前または生成後のレベルには影響しないため、外科的外傷の前に治療を行うことが不可欠です。 最近の総説では、著者はNSAIDによる術前治療を低リスクの患者では2日間、高リスクの患者では1週間行い、両群とも術後少なくとも4週間は継続することを推奨しています12
PCMEの予防や治療にどのNSAIDが最も効果的かについては、いまだに疑問があります。
ブロムフェナクナトリウム(Xibrom)やネパフェナクなどの新世代のNSAIDは、化学構造が変更されており、眼への浸透性や理論的な効力が高まっています13。in vitroのアッセイでは、COX-2阻害の相対的な効力はブロムフェナクがケトロラクの18倍であることがわかっていますが、このデータの臨床的な意義は不明です14。 生体内での薬物動態を調べたところ、市販のネパフェナク(ネパフェナク+アムフェナク)の房水濃度は、ブロムフェナクやケトロラクよりも有意に高いことが明らかになりました15。しかしながら、こうした浸透性の違いが臨床結果の改善につながるかどうかは不明です。
– 併用療法。 臨床的に重要なPCMEに対するケトロラック対プレドニゾロン対併用療法を評価した無作為化二重マスク前向き試験では、併用療法を受けた患者は2回目の診察までに平均2ライン以上の視力変化に達したのに対し、2つの単剤療法群の患者は3ヶ月後のフォローアップで平均2ラインの改善に達しなかったことがわかった16。 また、併用療法またはケトロラック単独療法を受けた患者は、プレドニゾロン群の患者よりも早く反応しました。
– コルチコステロイド注射。 コルチコステロイドはNSAIDsと同じ経路のさらに上流で働き、細胞膜のリン脂質からのアラカドン酸の放出を阻害することで、ロイコトリエンとプロスタグランジンの両方の形成を防ぎます(図1参照)。
最も効果的な投与経路(テノン下投与と眼内投与)、最適な投与量(4mgとそれ以上)、患者の安全性(眼圧上昇、網膜剥離、硝子体出血、眼内炎のリスク)などについて議論が続いています。
ある研究者グループは、持続性PCMEに対するtriamcinoloneのintravitrealは、視力の改善、黄斑部の厚さの減少、多焦点網膜電図の値の増加をもたらしたと報告しています17。 別の研究者は、慢性難治性PCMEに対してIVTA 4mgを使用したところ、注射後1ヵ月後に解剖学的および機能的な改善が得られ、少なくとも3ヵ月間はその効果が持続したと報告しています18。 さらに別の小規模なシリーズでは、難治性PCMEに対して4mg IVTAを単回投与した後、患者は視力の改善と黄斑部の厚さの減少を維持しました19
– アセタゾラミド。 アセタゾラミドは網膜下液の輸送を増加させ、網膜色素変性症、無水晶体、黄斑上膜形成などの疾患における小窩の嚢胞性浮腫を除去することが示されています20-23。アセタゾラミドの経口使用によりPCMEの解決に相関する症例報告がわずかにありますが、現在までに臨床試験は行われていません。
– 抗血管内皮増殖因子製剤。 外科的外傷は術後の炎症を引き起こし、血管内皮増殖因子などの血管透過性因子の産生を増加させることでPCMEを引き起こす可能性があります。 ここでも、小規模なケースシリーズでは矛盾した証拠が得られています。 ベバシズマブ(アバスチン)を硝子体内に注射したところ、あるグループでは71%の患者がETDRS視力を2本以上向上させたと報告しており24、また別のグループではすべての眼で統計的に有意な視力の改善が見られたと報告しています25。 臨床検査やOCTで機械的要素が確認されたPCMEの場合や、内科的治療に反応しない慢性難治性の浮腫の場合には、膜剥離を伴う柱状硝子体手術を検討することができる。 また、硝子体手術と内境界膜剥離により視力が改善したという症例報告もあります28。 先に述べたように、水晶体の破片が残っていたり、IOLの位置が悪かったり、P.acnesに感染していたりする場合には、パースプラナ硝子体手術を検討すべきです。
今後の方向性
前述したように、コルチコステロイドは炎症カスケードの初期に作用します。 ポスルデックス(アラガン社)は、生分解性のデキサメタゾン持続投与システムで、硝子体腔内に留置します。 ポリマーマトリックスが徐々に乳酸とグリコール酸に変化し、それらが水と二酸化炭素に分解されていく。 第2相試験では、PCMEおよびぶどう膜炎関連CME患者の54%が移植後90日目に10文字以上の視力改善を示したのに対し、観察群では14%しか同様の結果が得られませんでした。
最近、FDAは、手術中の眼内注射用に、トリアムシノロンアセトニドの「Triesence」(アルコン)を承認しました。
近年、PCMEの定義が進化していることが明らかになりました。 米国では年間約300万件の白内障手術が行われており、患者の期待も高まっていることから、網膜専門医にとっては、PCMEの多様な病因、危険因子、適切な管理方法を理解することが重要です。 新しい技術は、この疾患の診断、予後、治療に革命をもたらしましたし、今後もそうなるでしょう。
著者らはRetinal Consultants of Arizona(フェニックス)で診療を行っています。 また、Jamal博士はTexas Retina Associates(ダラス)、Goldenberg博士はAssociated Retinal Consultants(ロイヤルオーク、ミシガン)で診療しています。
1. Irvine SR. 白内障手術後に新たに定義された硝子体症候群。
2.Gass JD, Norton EW. 白内障抜去後の嚢胞性黄斑浮腫のフォローアップ研究。
3.Wright PL, Wilkinson CP, Balyeat HD, et al.後房レンズ移植後の血管造影による嚢胞性黄斑浮腫。
4.Henderson BA, Kim JY, Ament CS, et al.Clinical pseudophakic cystoid macular edema. 臨床的仮性嚢胞性黄斑浮腫の発症リスク要因と治療後の持続時間。 J Cataract Refract Surg 2007;33:1550-8.
5. McColgin AZ, Raizman MB. このようにして得られた結果が、今回の調査です。
6.Donnenfeld ED, Perry HD, Wittpenn JR, et al.超音波乳化術の成績における術前のケトロラク・トロメタミン0.4%。 Pharmacokinetic-response curve.
7.Almeida DR, Johnson D, Hollands H, Smallman D, et al.白内障手術後の光干渉断層計(Optical Coherence Tomography Quantification of Total Macular Volume)を用いて評価した嚢胞性黄斑浮腫に対する非ステロイド系抗炎症薬の予防的投与の効果。 J Cataract Refract Surg 2008;34:64-9.
8.Wittpenn JR, Silverstein S, Heier J, et al. A Randomized, Masked Comparison of Topical Ketorolac 0.4 percent Plus Steroid vs Steroid Alone in Low-Risk Cataract Surgery Patients. Am J Ophthalmol 2008; 146:554 -560.
9. Yavas GF, Oztürk F, Küsbeci T. 術前にインドメタシンを局所的に使用することで、仮性嚢胞性黄斑浮腫を防ぐことができます。 J Cataract Refract Surg 2007;33:804-7.
10. このような状況下では、このような問題を解決するためにはどうすればよいのでしょうか。 J Cataract Refract Surg 2007;33:1546-1549.
11. 小切開超音波乳化術および折り畳み式眼内レンズ挿入後の血管造影による嚢胞性黄斑浮腫および血液-水関門の破壊を軽減することができた。 ジクロフェナク0.1%とベタメタゾン0.1%の局所投与の多施設共同プロスペクティブ・ランダム化比較。 J Cataract Refract Surg 2008;34:57-63.
12. O’Brien TP. 白内障手術の患者ケアを最適化するためのNSAID療法の使用に関する新しいガイドライン。 Curr Med Res & Opin. 2005;21:1131-1137.
13. Walsh DA, Moran HW, Shamblee DA, et al. Antiinflammatory agents 3. 2-amino-3-benzoylphenylacetic acid and analoguesの合成と薬理学的評価. J Medicinal Chem 1984;27:1379-1388.
14. Waterbury LD, Silliman D, Jolas T. Comparison of cyclooxygenase inhibitory activity and ocular anti-inflammatory effects of ketorolac tromethamine and bromfenac sodium. Curr Med Res Opin 2006;22: 1133-1140.
15. このような状況の中で、私たちは、これまでの研究成果を活かして、より多くの人々に、より良い医療を提供していきたいと考えています。 J Cataract Refract Surg 2007;33;1539-1545.
16. このような状況の中で、私たちは、このような問題を解決するためにどのような取り組みを行っているのでしょうか。 Ophthalmology 2000;107:2034-8.
17. Koutsandrea C, Moschos MM, Brouzas D, et al.仮性嚢胞性黄斑浮腫に対する眼内のtriamcinolone acetonide。 光コヒーレンス・トモグラフィーと多焦点網膜電図の研究. Retina 2007;27:159-64.
18. 難治性の仮性嚢胞性黄斑浮腫に対するtriamcinolone acetonideの点滴静注。 機能的、解剖学的な結果。
19. 慢性仮性嚢胞性黄斑浮腫の治療のための硝子体内トリアムシノロンアセトニド。
20. Marmor MF. CMEの炭酸脱水療法に関する仮説:網膜上膜の例。
21. コックスSN、ヘイE、バードAC。 慢性黄斑浮腫のアセタゾラミドによる治療。
22. 網膜色素変性症における慢性黄斑浮腫の治療にアセタゾラミドを使用しています。
23. Wolfensberger TJ, Chiang R, Takeuchi A et al. Inhibition of membrane-bound carbonic anhydrase enhances subretinal fluid absorption and retinal adhesiveness. Graefe’s Arch Clin Exp Ophthalmol 2000; 238:76-80.
24. Arevalo JF, Garcia-Amaris RA, Roca JA, et al. 仮性嚢胞性黄斑浮腫の管理のための一次的なベバシズマブの眼内投与。 Pan-American Collaborative Retina Study Groupのパイロットスタディ。 J Cataract Refract Surg. 2007;33:2098-105.
25. このような状況の中で、私たちはどのようにしてこの問題を解決したのでしょうか? Retina 2008 Oct 9.
26. 術後の仮性嚢胞性黄斑浮腫に対するベバシズマブの有効性を検討しました。 J Cataract Refract Surg 2008;34:70-5.
27. 慢性仮性嚢胞性黄斑浮腫に対する硝子体手術。 Am J Ophthalmol 1999;128:317-23.
28. 慢性的な難治性の仮性嚢胞性黄斑浮腫に対する内境界膜剥離の効果。 A report of two cases. Am J Ophthalmol 2002;133:571-2.
。