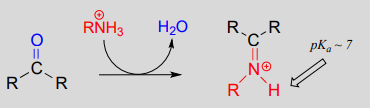
Het elektrofiele koolstofatoom van aldehyden en ketonen kan het doelwit zijn van nucleofiele aanval door zowel aminen als alcoholen. Het eindresultaat van een aanval door een nucleofiel amine is een functionele groep waarin de dubbele binding C=O is vervangen door een dubbele binding C=N, en die een imine wordt genoemd. (Een equivalente term is “Schiff base”, maar we zullen in dit boek “imine” gebruiken). Herinner je uit paragraaf 7.5B dat imines een pKa van ongeveer 7 hebben, dus bij fysiologische pH kunnen ze nauwkeurig worden getekend als ofwel geprotoneerd (iminium ion vorm) of neutraal (imine).
Iminiumionvorming:
Mechanisme (enzymatisch):
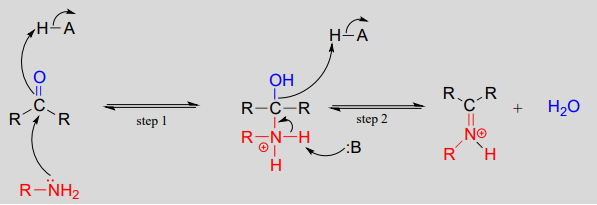
Mechanistisch gezien verloopt de vorming van een imine in twee stappen. Eerst valt de aminestikstof de carbonylkoolstof aan in een nucleofiele additiestap (stap 1) die nauw analoog is aan hemiacetaal- en hemiketaalvorming. Op basis van je kennis van het mechanisme van de vorming van acetalen en ketalen zou je verwachten dat de volgende stap de aanval door een tweede amine zou zijn om een verbinding te vormen met een koolstof die gebonden is aan twee aminogroepen – de stikstofversie van een ketaal of acetaal. Maar wat er daarna gebeurt (stap 2 hierboven) is dat de eenpaarelektronen van stikstof de zuurstof van de koolstof ‘duwen’, waardoor een dubbele binding (een iminium) en een ontheemde watermolecule worden gevormd.
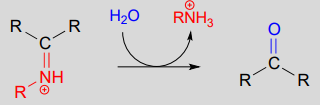
De omzetting van een iminium terug naar een aldehyde of keton is een hydrolytisch proces (bindingen worden verbroken door een watermolecuul), en is mechanistisch gezien gewoon het omgekeerde van iminiomvorming:
Hydrolyse van een iminiumion:
Mechanisme (enzymatisch):
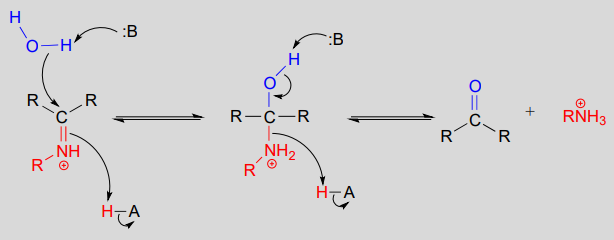
Koolstof-koolstofbinding vormende enzymen, aldolases genaamd (die we in hoofdstuk 12 in detail behandelen), vormen vaak iminiumverbindingen tussen een carbonylkoolstof op een substraat en een lysineresidu uit de actieve site van het enzym, zoals in deze aldolase-reactie uit de Calvijncyclus:
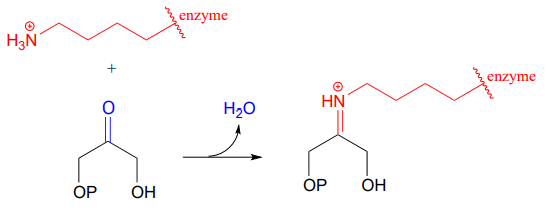
Nadat de koolstof-koolstofverbinding die deel uitmaakt van een aldolase-reactie is voltooid, wordt de iminiumkoppeling gehydrolyseerd, waarbij het product vrijkomt, zodat het uit de actieve site kan diffunderen en een nieuwe katalytische cyclus kan beginnen.
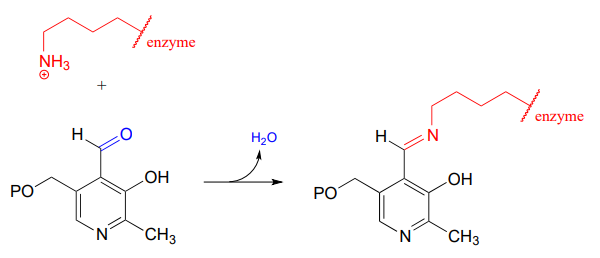
Daarna wordt de \(PLP\)-lysine-iminebinding ingeruild voor een iminebinding tussen \(PLP\)-lysine en de aminogroep op het substraat, in wat kan worden aangeduid als een transiminatie.
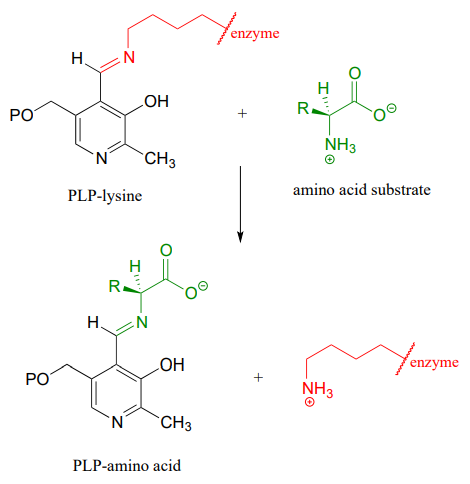
Het mechanisme voor een transiminatie lijkt sterk op dat van de vorming van imines:
Transimineringsreactie:
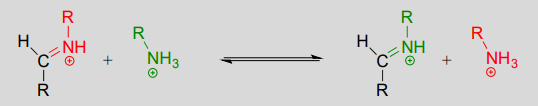
Mechanisme:
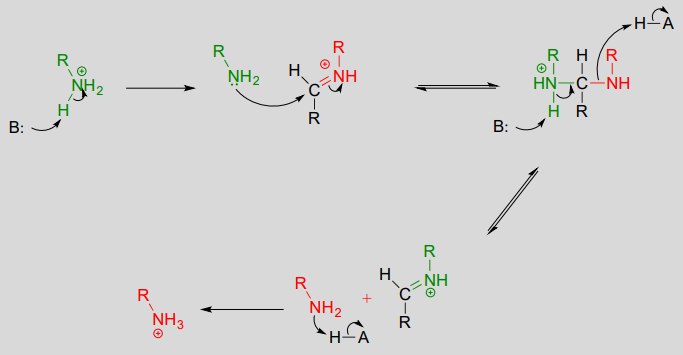
Oefening(PaginaIndex{1})
Teken een imine dat tussen elk paar verbindingen gevormd zou kunnen worden.
a.
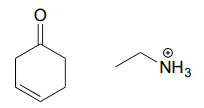
b.
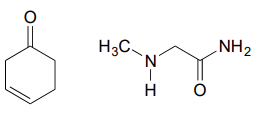
c.
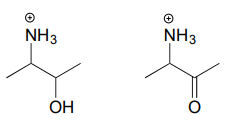
Oefening (Pagina-index{2})
Teken het imminiumhydrolyseproduct voor elk van de volgende verbindingen.
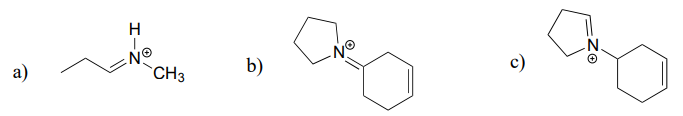
Antwoord
Voeg hier de antwoordtekst in en deze wordt automatisch verborgen als je een “AutoNum”-sjabloon op de pagina actief hebt.
Oefening
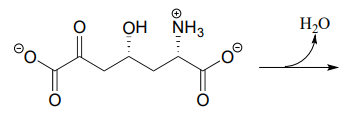
- Het hieronder afgebeelde metabole tussenproduct ondergaat een intramoleculaire iminevorming als stap in de biosynthese van lysine (EC 4.3.3.7). Teken het product van deze intramoleculaire imine vorming stap.
- Voorspel het product van deze iminehydrolysestap (EC 2.3.1.117) uit de afbraakroute van proline.
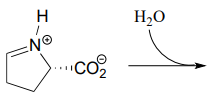
Contributors
-
Organic Chemistry With a Biological Emphasis door Tim Soderberg (Universiteit van Minnesota, Morris)