Casusverslag
Behandeling van proliferatief baarmoederslijmvlies bij biopsie bij postmenopauzale vrouwen
Sidharth Srinivas1, Sachchidananda Maiti2, Perunkulam Jothilakshmi2
1Manchester Medical School, University of Manchester, Manchester, Verenigd Koninkrijk
2Obstetrie & Gynaecologie, The Pennine Acute NHS Hospitals, Crumpsall, Verenigd Koninkrijk
Emailadres:
 (S. Srinivas)
(S. Srinivas) Om dit artikel te citeren:
Sidharth Srinivas, Sachchidananda Maiti, Perunkulam Jothilakshmi. Management van proliferatief endometrium op biopsie in post-menopauzale vrouwen. Tijdschrift voor Gynaecologie en Verloskunde. Vol. 4, No. 6, 2016, pp. 38-43. doi: 10.11648/j.jgo.20160406.12
Ontvangen: 4 september 2016; Geaccepteerd: 21 september 2016; Gepubliceerd: 15 oktober 2016
Abstract: Postmenopauzaal bloedverlies (PMB) wordt meestal veroorzaakt door verschillende endometriumaandoeningen (hyperplasie en carcinoom) waarvoor evidence-based behandelingen bestaan. Er is echter weinig literatuur en geen evidence-based behandeling voor het vinden van proliferatief endometrium zonder atypie op Pipelle endometrium biopsie bij vrouwen die zich presenteren met PMB. Ons doel is om het management en de behandelingsopties voor deze subgroep van vrouwen te onderzoeken. Dit is een retrospectieve, observationele casusbespreking van vrouwen die zich met PMB meldden bij een gynaecologische spoedkliniek in een algemeen ziekenhuis in Manchester, Verenigd Koninkrijk, gedurende een periode van drie weken. Vier vrouwen bij wie een proliferatief of secretorisch endometrium werd gevonden op een endometriale Pipelle biopsie werden gekozen. Hun voorgeschiedenis, onderzoeksbevindingen, onderzoeken, behandeling en vervolgbevindingen werden vervolgens geanalyseerd. Deze case-serie heeft het dilemma geïdentificeerd van patiënten met proliferatief endometrium zonder atypie op de endometriumstalen. De vier patiënten werden opgevolgd met een herhaalde Pipelle endometriumbiopsie zes weken na presentatie op de gespecialiseerde afdeling gynaecologie. Zij kregen vervolgens advies of werden gedurende zes tot acht weken behandeld met orale progesterontherapie. De behandelingsopties omvatten het Mirena intra-uteriene systeem (IUS), orale progesterontherapie en ontslag van de patiënte naar de eerstelijnsgezondheidszorg. Er is geen consensus over het belang van oraal progesteron of de duur van de follow-up die nodig is om te controleren op de ontwikkeling van endometriumhyperplasie of kanker bij deze subgroep van patiënten. Verder onderzoek is nodig om evidence-based, management richtlijnen te ontwikkelen voor proliferatief endometrium bij vrouwen met PMB.
Keywords: Post-Menopauzale Bloedingen, Proliferatief Endometrium Zonder Atypie, Progesteron Therapie
1. Inleiding
Postmenopauzale bloedingen zijn een belangrijke en veel voorkomende presentatie in de gynaecologische kliniek. Dringend onderzoek is noodzakelijk om endometriumkanker – de meest voorkomende gynaecologische maligniteit in het Verenigd Koninkrijk – uit te sluiten. Goedaardige oorzaken zoals atrofische vaginitis, poliepen en vleesbomen kunnen de patiënte ook veel stress bezorgen. Een histologische diagnose van endometriumhyperplasie verhoogt het risico op maligniteit en behandeling is vereist om regressie te induceren. Daarentegen laat een histologische diagnose van proliferatief endometrium zonder atypische cellen clinici zonder evidence-based behandeling en onzekerheid over het potentieel voor maligne transformatie.
In dit rapport hebben we vier gevallen van PMB geanalyseerd waarbij bij onderzoek proliferatief endometrium werd gevonden op histologie. Deze case serie is van belang omdat er een tekort is aan literatuurgegevens over proliferatief endometrium bij postmenopauzale vrouwen die zich presenteren met een symptoom van PMB, en als gevolg daarvan geen evidence-based behandeling. Dit rapport zal gebieden van onzekerheid in ons begrip en beheer van deze patiënten identificeren.
Methoden
Dit is een retrospectieve, observationele case-serie waarbij wordt gekeken naar vrouwen die zich in november 2014 met PMB presenteerden op een snelle toegangskliniek voor gynaecologie (RAC) in een districtsgeneraal ziekenhuis in Manchester over een periode van 3 weken. Vier patiënten die proliferatief of secretorisch endometrium bleken te hebben bij endometriale bemonstering met een Pipelle-apparaat werden willekeurig gekozen. De postmenopauzale vrouwen in deze case-serie werden allemaal met spoed doorverwezen naar de secundaire zorg na het ervaren van ten minste één episode van bloeding. In deze case-serie werden vrouwen van alle leeftijden opgenomen die een natuurlijke menopauze hadden doorgemaakt. Aan de hand van casusbeschrijvingen werden de voorgeschiedenis, onderzoeksresultaten, onderzoeken, behandeling en follow-up van elke patiënt geanalyseerd.
2. Casusreeks
Tabel 1. Relevante aspecten van de voorgeschiedenis van de patiënt.
| Patiënt | Leeftijd & Menopausale status | Reden voor verwijzing | Geassocieerde symptomen | Verleden medische geschiedenis | Contraceptie, HRT &status tamoxifen | Historie baarmoederhalsuitstrijkje |
| 1 | 54, post-menopauze sinds 2 jaar | Twee hevige periodes van bloedingen gedurende telkens vijf dagen | Buikinaal ongemakken | Nihil | Nihil | Normaal & up-tot op heden |
| 2 | 59, sinds 5 jaar postmenopauzaal | Tien dagen hevig vaginaal bloedverlies met stolsels | Ongemak in de onderbuik en gewichtsverlies | Diabetes mellitus type 2, hoge bloeddruk en galstenen | GP gestart met Norethisteron voor bloedingen | Normaal & up-tot-date |
| 3 | 52, postmenopauzaal 1 jaar | Onregelmatig dik baarmoederslijmvlies op echo bij eerstelijnszorg | Intermitterende bloedingen met stolsels en overstromingen | Borstkanker, bi-laterale mastectomie en okselklierverwijdering | Mirena IUS en Tamoxifen één jaar geleden | Normaal & up-tot-date |
| 4 | 59, post-menopauzaal | Acht dagen aanhoudend licht vaginaal bloedverlies | Milde buikpijn | Hypertensie, hyperthyreoïdie, verhoogde body mass index | Nihil | Onbekend |
Tabel 2. Onderzoeksresultaten en behandeling.
| Patiënt | Pelvic onderzoek & TVUS | Hysteroscopie | Pipelbiopsie | Herhaalde pipelle biopsie | Behandeling | Duur van opvolgingup | |
| 1 | Normaal & 1. Behandeling | Normaal &3mm | Niet uitgevoerd | Proliferatief endometrium zonder atypie of maligniteit | Secretair endometrium zonder atypie of maligniteit | MDPA 100mg BD gedurende 6 tot 8 weken | 6 weken |
| 2 | Normaal & 10mm | Normaal afgezien van 2.5mm polypoïdale poliep | Secretair endometrium zonder atypie of maligniteit | Proliferatief endometrium zonder atypie of maligniteit | Mirena IUS counseling | 6 weken | |
| 3 | 2mm | Niet uitgevoerd | Proliferatief endometrium zonder atypie of maligniteit | Proliferatief endometrium zonder atypie of maligniteit | Nihil | 8 weken | |
| 4 | Normaal & 10mm | Normaal afgezien van een kleine poliep | Proliferatief baarmoederslijmvlies zonder atypie of maligniteit | Proliferatief baarmoederslijmvlies zonder atypie of maligniteit | MDPA 100mg BD gedurende 6 tot 8 weken | 8 weken |
3. Discussie
3.1. Endometriale veranderingen tijdens de menopauze
Een endometrium dat atrofieert en zijn functionele laag verliest, met endometriaal stroma dat fibreus wordt en klieren die noch proliferatieve noch secretorische activiteit vertonen – is het geaccepteerde beeld van het postmenopauzale endometrium. Deze regressie van het endometrium valt samen met het ophouden van de menstruatie, zodat pathologie moet worden uitgesloten wanneer bloedingen optreden. De fysiologie van het postmenopauzale endometrium en zijn rol in de pathologie van het bekken heeft de laatste decennia de aandacht getrokken, met bijzondere aandacht voor de voorlopers van endometriumcarcinoom. Er is echter veel minder literatuur over het postmenopauzale endometrium in vergelijking met het endometrium tijdens het reproductieve leven.
In het algemeen hebben studies aangetoond dat driekwart van de postmenopauzale vrouwen een geatrofieerd endometrium blijkt te hebben met een variërende mate van uitgezette cysteuze klieren. Nog eens 15% heeft endometriale poliepen die uit cystische klieren bestaan. Endometrium met proliferatie en hyperplasie is goed voor de resterende 10%. Atrofie van het baarmoederslijmvlies komt voor in het eerste jaar van de menopauze en de incidentie blijft constant gedurende de menopauze. In tegenstelling tot de gevallen van proliferatie en hyperplasie die vooral in de eerste 5 jaar na de menopauze worden gezien.
In 1954 analyseerde McBride het endometrium na de menopauze in een groot onderzoek; hij nam met behulp van curettage monsters van 1.521 patiënten in verschillende perioden na de menopauze. In 1.315 monsters werd weinig materiaal dan slijm verkregen, terwijl de overige 206 gevallen de volgende endometriale patronen vertoonden: atrofie, enkele of diffuse cysteuze klier, hyperplasie, proliferatie, secretoire en fibro-adenomateuze poliepen. De resultaten suggereren dat de incidentie van proliferatief of secretorisch endometrium 6,3% bedraagt. De auteur stelt echter voor dat wanneer geen monster werd verkregen, het endometrium ofwel inactief ofwel geatrofieerd was. In deze veronderstelling is de incidentie van proliferatief of secretief baarmoederslijmvlies 0,8%. Dit leidt tot de veronderstelling dat de werkelijke incidentie van proliferatief of secretorisch endometrium tussen 6,3% en 0,9% ligt.
Een onderzoek naar endometriale biopsieën van peri- en postmenopauzale vrouwen die continu HRT gebruikten, toonde aan dat de meerderheid van de endometrium ofwel atrofisch (68,7%) ofwel proliferatief (23,5%) zijn. Terwijl 0,6% eenvoudige hyperplasie zonder atypie vertoonde, had 0,5% secretorisch endometrium en goed gedifferentieerd adenocarcinoom werd gevonden in 0,07% van de gevallen. Dit suggereert dat postmenopauzale vrouwen die hormonaal gestimuleerd worden een hogere incidentie van proliferatief endometrium hebben.
3.2. Oorzaken van postmenopauzale bloedingen
Postmenopauzale bloedingen zijn vaginale bloedingen bij een postmenopauzale vrouw die niet de verwachte cyclische bloedingen zijn die optreden bij sequentiële hormoonvervangingstherapie. PMB moet dringend worden doorverwezen naar de gynaecologie omdat 10% van deze patiënten endometriumkanker heeft. Een vroege diagnose van endometriumkanker is belangrijk om lokale en kwaadaardige verspreiding te verminderen en wordt geassocieerd met een overleving tot 90% . Endometriumkanker presenteert zich vaak in een vroeg stadium met PMB, maar atrofische vaginitis en goedaardige laesies zoals poliepen en fibromen komen ook vaak voor. Uit een studie bleek dat tot 30% van de gevallen van PMB een onderliggende anatomische afwijking vertoont (zie tabel 3).
Tabel 3. De anatomische oorzaken van postmenopauzale bloedingen.
| Endometrium | Cervix | Vagina | Ovararium |
| Fibroïden | Poliepen | Atrofische vaginitis | Kanker |
| Hyperplasie | Kanker | Kanker | Polyps | Kanker |
| Endometritis |
3.3. Onderzoek naar postmenopauzale bloedingen
In overeenstemming met de richtlijnen van het National Institute of Clinical Excellence (NICE) werden drie van de patiënten in onze casusreeks die zich met PMB presenteerden en geen HRT gebruikten, allemaal doorverwezen naar de tweedelijnsgezondheidszorg om kanker uit te sluiten. Deze patiënten werden allemaal binnen 2 weken op een gynaecologische polikliniek gezien – waarmee de nationale doelstelling voor dringende verwijzingen werd gehaald.
Patiënten die worden behandeld met HRT zijn complexer, omdat het moeilijk kan zijn om onderscheid te maken tussen normale cyclische en onregelmatige bloedingen. Baarmoederbloedingen of spotting bij het starten van HRT zijn normaal, maar zouden na 6 maanden moeten stoppen. NICE beveelt echter een dringende verwijzing aan voor aanhoudende of onverklaarde postmenopauzale bloedingen na het staken van HRT gedurende 6 weken.
Het Scottish Intercollegiate Guidelines Network (SIGN) biedt een algoritme voor het onderzoek van PMB (zie tabel 4). In overeenstemming met deze richtlijnen kregen alle vier de patiënten een bekkenonderzoek om te zoeken naar goedaardige oorzaken van de bloeding, zoals cervicale ectropionen of poliepen, of om de verdenking van maligniteit te verhogen. Een grondige anamnese met identificatie van risicofactoren voor endometriumkanker zoals een voorgeschiedenis van chronische anovulatie, obesitas, diabetes, gebruik van oestrogeen of tamoxifen en genetische syndromen is waardevol. Bovendien stelt een speculumonderzoek ervaren clinici in staat om vulval-, vaginale en cervicale laesies te diagnosticeren. Een grondige anamnese en een grondig onderzoek kunnen ook de verdenking doen rijzen van zeldzame oorzaken van vaginaal bloedverlies, zoals stollingsstoornissen en leukemie.
Zoals aanbevolen door SIGN, was TVUS het eerstelijnsonderzoek dat werd gebruikt voor vrouwen die zich in onze case-serie presenteerden met PMB. Door de onderbouwing, het gemak en het ontbreken van complicaties is het een ideaal onderzoek om patiënten met een verhoogd risico op kanker te beoordelen. Bij dikker endometrium neemt het risico op pathologie, zoals maligniteit, toe, hetgeen nader onderzoek rechtvaardigt. Terwijl vrouwen met dun baarmoederslijmvlies kunnen worden gerustgesteld en alleen voor verder onderzoek kunnen worden opgeroepen als de bloeding aanhoudt . Bij de vaststelling van de afkapwaarde voor de endometriumdikte moet een evenwicht worden gevonden tussen de noodzaak om alle sinistere pathologieën op te sporen en het minimaliseren van het overmatig gebruik van middelen. Door de afkapwaarde op 3 mm vast te stellen, wordt een hoge sensitiviteit (100%) bereikt, maar wordt de specificiteit (25,8%) van het onderzoek aangetast, waardoor een te groot aantal patiënten wordt onderzocht. Momenteel wordt in de klinische praktijk 4 mm gebruikt omdat dit de optimale sensitiviteit (91,6%) en specificiteit (44,5%) wordt geacht te bieden.
Er zijn ook andere vormen van echografie beschikbaar, zoals transvaginale doppler, driedimensionale, met zoutoplossing versterkte en het meten van de endometriale textuur en margeanalyse. Studies hebben echter geen voordelen ten opzichte van TVUS aangetoond en worden momenteel niet aanbevolen of gebruikt in de klinische routinepraktijk
Directe inspectie en bemonstering van endometriumweefsel wordt beschouwd als de gouden standaard en de tweede onderzoekslijn in dit cohort van patiënten. In de huidige praktijk en SIGN-richtlijnen wordt het gebruik van endometriale biopsieapparatuur aanbevolen voor verder onderzoek van patiënten bij wie het risico op endometriumkanker hoger wordt geacht. Traditioneel werd dilatatie & curettage gebruikt om abnormale bloedingen te onderzoeken, maar er is nu bewijsmateriaal voor het gebruik van endometriale bemonsteringsapparaten zoals het Pipelle-apparaat – gebruikt bij alle vier de patiënten in mijn casuserie. Het heeft een detectiegraad van 99,6% voor endometriumkanker bij postmenopauzale vrouwen, evenals een hoge sensitiviteit (81%) en specificiteit (98%) voor het identificeren van atypische hyperplasie. Samenvattend biedt een combinatie van TVUS en Pipelle endometriale biopsie voldoende diagnostische informatie om benigne en maligne endometriumziekte te diagnosticeren of uit te sluiten.
Patiënten die worden behandeld met tamoxifen hebben een drie tot zes keer hogere incidentie van endometriumkanker, en een dringende verwijzing voor dergelijke vrouwen die klagen over PMB wordt aanbevolen door NICE . Het is aangetoond dat het risico op kanker en proliferatie, als gevolg van het zwakke oestrogene effect van tamoxifen, toeneemt met toenemende dosis en duur van de behandeling. Patiënte 3 in onze case-serie, een 59-jarige vrouw die tamoxifen gebruikte, werd uitgebreider onderzocht door middel van hysteroscopie in aanvulling op een TVUS en Pipelle-biopsie. Dit is in overeenstemming met de richtlijnen die suggereren dat hysteroscopie met biopsie de voorkeur verdient boven TVUS, omdat de interpretatie van ultrasonografie wordt bemoeilijkt door endometriale verdikking bij patiënten die tamoxifen gebruiken.
Tabel 4. Vrouwen die zich presenteren met bloedingen na de menopauze (en die geen tamoxifen gebruiken).
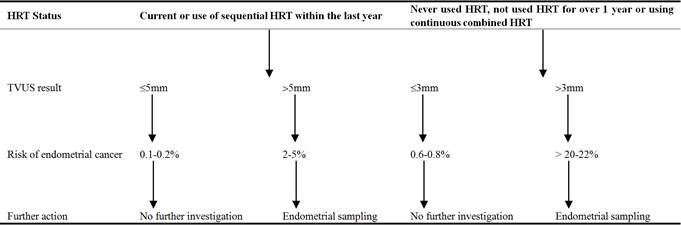
3.4. Endometriumhyperplasie
De diagnose endometriumhyperplasie (EH) wordt gesteld bij ongeveer 10% van de vrouwen die zich met PMB presenteren. De Wereldgezondheidsorganisatie (WHO) deelt endometriumhyperplasie in in eenvoudige en complexe typen; elk type wordt vervolgens verder ingedeeld naar de aan- of afwezigheid van nucleaire atypie. Vrouwen bij wie bij een endometriale biopsie atypie (zie figuur 2) wordt vastgesteld, moeten nader worden onderzocht, aangezien ongeveer 50% tegelijkertijd endometriumcarcinoom heeft. Bovendien is het risico van kanker verhoogd bij aanwezigheid van atypie (27,5% na 9 jaar na diagnose), maar veel lager bij hyperplasie zonder atypie (4,6% na 9 jaar na diagnose). Gezien de waarschijnlijkheid van toekomstige maligniteit, wordt hysterectomie met bilaterale salpingo-oophorectomie aanbevolen bij postmenopauzale vrouwen met EH in aanwezigheid van atypie. Als er geen atypische cellen zijn, kunnen vrouwen worden behandeld met progestativa en seriële biopsieën om de 6 maanden om de respons op de behandeling te verzekeren. Veel gebruikte progestativa zijn megestrolacetaat en medroxyprogesteronacetaat. Hoewel de vier patiënten in onze case-serie geen endometriumhyperplasie hebben, kan worden verondersteld dat als er atypische cellen waren gevonden, het risico op maligniteit en de noodzaak van verder onderzoek zou zijn toegenomen bij patiënten met proliferatief of secretorisch endometrium.
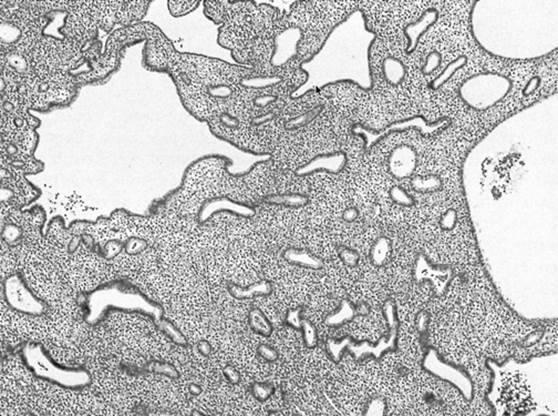
Figuur 1. Een endometriaal biopt toont eenvoudige endometriumhyperplasie, met onregelmatig verdeelde endometriumklieren die wijd gescheiden zijn door hyperplastisch stroma.
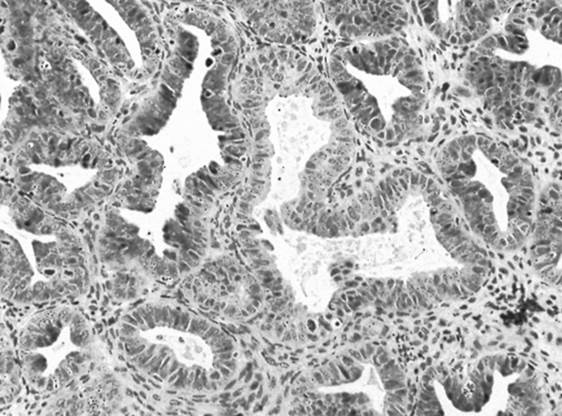
Figuur 2. Een endometriale biopsie met endometriumhyperplasie met atypische kliercellen
3.5. Pathogenese van proliferatief endometrium
Mijn rapport heeft postmenopauzale vrouwen geïdentificeerd bij wie de biopten het endometrium imiteerden dat wordt aangetroffen in de maandelijkse menstruatiecyclus van een reproductieve vrouw. Verhoogde mitotische activiteit van het stromale epitheel gepaard gaande met cellulaire hyperplasie en verhoogde extracellulaire matrix resulteren in verdikking van het endometrium tijdens de proliferatieve fase van het endometrium (zie figuur 3). Deze proliferatie wordt gestimuleerd door oestrogeen dat tijdens de menstruatiecyclus door zich ontwikkelende follikels wordt afgescheiden. Progesteron werkt de werking van oestrogeen tegen en stopt de proliferatieve fase van de endometriumcyclus. Progesteron induceert de secretiefase door de endometriumklieren te stimuleren en de vasculariteit te verhogen (zie figuur 4). De dikte van het baarmoederslijmvlies neemt verder toe naarmate de klieren, stromale cellen en bloedvaten volgroeien. Bij postmenopauzale vrouwen wordt aangenomen dat lage niveaus van oestrogeen en progesteron uit extra-folliculaire bronnen het baarmoederslijmvlies stimuleren tot proliferatie. Bovendien zijn fyto-oestrogenen, zoals oliehoudende zaden, sojaproducten en tofu, plantaardige stoffen die structureel en functioneel vergelijkbaar zijn met oestradiol. Ondanks studies die suggereren dat fyto-oestrogenen geen proliferatie induceren noch het risico van endometriumkanker verhogen, zijn hun langetermijneffecten relatief onbekend. Evenzo bestaat er onzekerheid over het vrij verkrijgbare gebruik van zwarte cohosh – een kruidenmiddel met mogelijke proliferatieve effecten op het baarmoederslijmvlies.
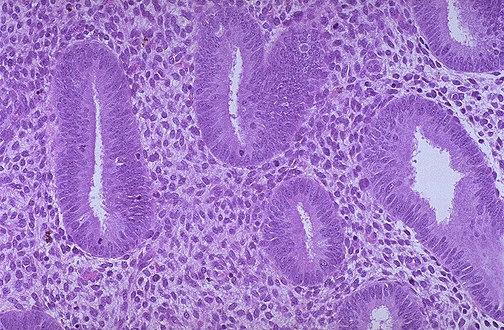
Figuur 3. De microscopische verschijning van proliferatief endometrium, met proliferatie van buisvormige klieren en dicht stroma .
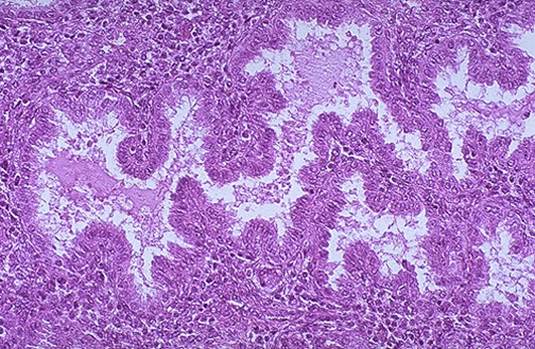
Figuur 4. De microscopische verschijning van secretorisch endometrium en grote kronkelige klieren gevuld met afscheiding
Studies hebben aangetoond dat proliferatief endometrium niet ongewoon is en suggereren ook dat kankers van het endometrium voortkomen uit een achtergrond van proliferatieve activiteit en niet inertie . De waarschijnlijkheid dat eenvoudig proliferatief endometrium zich ontwikkelt tot maligniteit is echter zeer laag en aanzienlijk lager dan het risico van 0,3 tot 1% dat endometriumhyperplasie zich ontwikkelt tot kanker . Risicofactoren zijn echter een verhoogde body mass index en leeftijd. Beide worden geassocieerd met perifere aromatisatie en veel voorkomende co-morbiditeiten bij patiënten met endometriumkanker.
3.6. Behandeling van proliferatief endometrium
Voor zover wij weten zijn er geen studies gepubliceerd over de behandeling van endometriumproliferatie zonder atypie bij postmenopauzale bloedingen. Als gevolg hiervan is er momenteel geen evidence-based behandeling voor dergelijke vrouwen. Er is ook geen consensus over de aanbevolen dosis en duur van de behandeling met MDPA bij deze subgroep van patiënten. Bovendien bestaat er geen overeenstemming over de frequentie van de follow-up die nodig is om sinistere endometriale proliferatieve pathologieën uit te sluiten.
Er zijn een paar stromingen onder gynaecologen over hoe deze patiënten het beste kunnen worden behandeld. Aangezien het risico dat proliferatief endometrium in kanker verandert zeer laag wordt geacht, is een optie de patiënte gerust te stellen alvorens haar terug te sturen naar de eerstelijnsgezondheidszorg. Een meer conservatieve aanpak daarentegen is het gebruik van systemische progesterontherapie om regressie van het endometrium te induceren. Oraal medroxyprogesteronacetaat kan voor een relatief korte periode (zes tot acht weken in onze gevallen) worden voorgeschreven om endometriumregressie te bewerkstelligen. De voordelen van progesterontherapie moeten zorgvuldig worden afgewogen tegen de bijwerkingen, zoals het risico van diep-veneuze trombose. Een optie voor de langere termijn die door sommige gynaecologen wordt overwogen is het Mirena intra-uteriene systeem, een langwerkende omkeerbare vorm van anticonceptie die het baarmoederslijmvlies verdunt door afgifte van progesteron in de baarmoeder. Beide vormen van progesteron worden ook gebruikt bij endometriumhyperplasie en het is aangetoond dat zij het endometrium beschermen tegen proliferatie en kwaadaardige transformatie . Mirena IUS heeft een vergunning om endometriale bescherming te bieden gedurende 4 jaar. De tweede patiënte in onze case-serie werd gestart met progesterontherapie nadat bij één Pipelle-biopsie proliferatief endometrium was gevonden, terwijl de vierde patiënte met dezelfde behandeling werd gestart na bevestiging van histologie met een herhaalde Pipelle-biopsie. Door het gebrek aan bewijs is het onzeker of een herhaalde biopsie nodig is om de bevindingen te bevestigen, dan wel of een enkele biopsie voldoende is voor behandeling. Wij stelden ook vast dat patiënten in onze case series gedurende 6 tot 8 weken werden behandeld met oraal medroxyprogesteron, maar voor zover wij weten heeft geen enkele studie gekeken naar de ideale duur van de behandeling. Een meer radicale benadering van proliferatief endometrium zou een hysterectomie zijn bij herhaalde episoden van PMB om elk risico van transformatie in endometriumcarcinoom uit te sluiten. De anesthesie, operatierisico’s en psychologische impact maken dit echter tot het laatste redmiddel. Bij drie van de vier patiënten werd binnen 6 weken een follow-up en herhaalde Pipelle endometriumbiopsie verricht. Er zijn echter geen gegevens over de frequentie van de follow-up of de beoordeling van de respons op de behandeling. Bovendien is het onduidelijk of risicofactoren zoals hoge BMI en borstkanker de drempel voor het aanbieden van een herhaalde Pipelle-biopsie moeten verlagen.
4. Conclusie
Dit rapport heeft de huidige trends in het beheer van proliferatief endometrium met oraal medroxyprogesteron in kaart gebracht. Meerdere gebieden van onzekerheid zoals de duur van de behandeling en de follow-up zijn naar voren gebracht. Meer onderzoek naar proliferatief endometrium bij PMB is nodig om evidence-based behandelingsrichtlijnen te ontwikkelen.
- UK CR. Kankerstatistieken: Registrations Series. 2011.
- McBride. The normal post-menopausal endometrium. J Obstet Gynaecol Br Emp 1954;61 (5):691-7.
- Noer T. De histologie van het seniele endometrium. Acta Pathologica Microbiologica Scandinavica 1961;51 (3):193.
- Korhonen MO, Symons JP, Hyde BM, Rowan JP, Wilborn WH. Histologic classification and pathologic findings for endometrial biopsy specimens obtained from 2964 perimenopausal and postmenopausal women undergoing screening for continuous hormones as replacement therapy (CHART 2 Study). American Journal of Obstetrics and Gynecology 1997;176 (2):377.
- Goldstein RB, Bree RL, Benson CB, Benacerraf BR, Bloss JD, Carlos R, et al. Evaluation of the woman with postmenopausal bleeding: Society of Radiologists in Ultrasound-Sponsored Consensus Conference statement. J Ultrasound Med 2001;20 (10):1025-36.
- SIGN. Onderzoek naar postmenopauzale bloedingen. 2002.
- Paley PJ. Screening op de belangrijkste maligniteiten bij vrouwen: Huidige richtlijnen. American journal of obstetrics and gynecology 2001;184 (5):1021.
- NICECG27. Verwijsrichtlijnen bij Vermoeden van Kanker. 2005.
- Nand SL, Webster MA, Baber R, O’Connor V. Bloedingspatroon en endometriale veranderingen tijdens continue gecombineerde hormoonvervangingstherapie. The Ogen/Provera Study Group. Obstet Gynecol 1998;91 (5 Pt 1):678-84.
- Davidson KG, Dubinsky TJ. Ultrasonografische evaluatie van het endometrium bij postmenopauzale vaginale bloedingen. Radiol Clin North Am 2003;41 (4):769-80.
- Gupta JK, Chien PFW, Voit D, Clark TJ, Khan KS. Ultrasonografische endometriumdikte voor de diagnose van endometriale pathologie bij vrouwen met postmenopauzale bloedingen: een meta-analyse. Acta Obstetricia et Gynecologica Scandinavica 2002;81 (9):799.
- Dijkhuizen FPHLJ, BrÃ-Lmann HAM, Potters AE, Bongers MY, Heintz APM. The Accuracy of Transvaginal Ultrasonography in the Diagnosis of Endometrial Abnormalities. Obstetrics & Gynaecology 1996;87 (3):345-349.
- Ciatto S, Cecchini S, Gervasi G, Landini A, Zappa M, Crocetti E. Surveillance for endometrial cancer with transvaginal ultrasonography of breast cancer patients under tamoxifen treatment. Br J Cancer 2003;88 (8):1175-9.
- Weber G, Mere E, Bahlmanw E, Riisch B. Evaluatie van verschillende transvaginale sonografische diagnostische parameters bij vrouwen met postmenopauzale bloedingen. Echografie in Obstetrie en Gynaecologie 1998;12 (4):265.
- Gruboeck K, Jurkovic D, Lawton F, Savvas M, Tailor A, Campbell S. De diagnostische waarde van endometriale dikte- en volumemetingen door middel van driedimensionale echografie bij patiënten met postmenopauzale bloedingen. Echografie in Obstetrie en Gynaecologie 1996;8 (4):272.
- Dijkhuizen FPHLJ, Mol BWJ, Brölmann HAM, Heintz APM. The accuracy of endometrial sampling in the diagnosis of patients with endometrial carcinoma and hyperplasia. Cancer 2000;89 (8):1765.
- Van den Bosch T, Vandendael A, Van Schoubroeck D, Wranz PA, Lombard CJ. Combining vaginal ultrasonography and office endometrial sampling in the diagnosis of endometrial disease in postmenopausal women. Obstet Gynecol 1995;85 (3):349-52.
- Curtis RE, Boice JD, Shriner DA, Hankey BF, Fraumeni JF. Second Cancers After Adjuvant Tamoxifen Therapy for Breast Cancer. Journal of the National Cancer Institute 1996;88 (12):832-835.
- Karlsson B, Granberg S, Wikland M, Torvid K, Marsal K, et al. Transvaginale ultrasonografie van het endometrium bij vrouwen met postmenopauzale bloedingen âa Nordic multicenter study. American Journal of Obstetrics and Gynecology 1995;172 (5):1488.
- Lacey JV, Chia VM. Endometriale hyperplasie en het risico van progressie naar carcinoom. Maturitas 2009;63 (1):39.
- Lacey JV, Sherman ME, Rush BB, Ronnett BM, Ioffe OB, Duggan MiA, et al. Absolute Risk of Endometrial Carcinoma During 20-Year Follow-Up Among Women With Endometrial Hyperplasia. Journal of Clinical Oncology 2010;28 (5):788-792.
- Silverberg. Tumoren van het baarmoederlichaam en trofoblastische zwangerschapsziekte. AFIP Atlas of Tumor Pathology 1995.
- Balk JL, Whiteside DA, Naus G, DeFerrari E, Roberts JM. A pilot study of the effects of phytoestrogen supplementation on postmenopausal endometrium. J Soc Gynecol Investig 2002;9 (4):238-42.
- Pathologie FG. http://library.med.utah.edu/WebPath/FEMHTML/FEMIDX.html#2.
- Sivridis E, Giatromanolaki A. Proliferative activity in postmenopausal endometrium: the lurking potential for giving rise to an endometrial adenocarcinoma. J Clin Pathol 2004;57 (8):840-4.
- Baak JP, Wisse-Brekelmans EC, Fleege JC, van der Putten HW, Bezemer PD. Beoordeling van het risico op endometriumkanker bij hyperplasie, aan de hand van morfologische en morfometrische kenmerken. Pathol Res Pract 1992;188 (7):856-9.
- Wan YL, Holland C. The efficacy of levonorgestrel intrauterine systems for endometrial protection: a systematic review. Climacteric;14 (6):622-632.