Leerdoelen
- Leer de basistermen die worden gebruikt om materie te beschrijven.
De definitie van scheikunde – de studie van de interacties van materie met andere materie en met energie – gebruikt enkele termen die ook gedefinieerd moeten worden. We beginnen de studie van de scheikunde met de definitie van enkele basistermen.
Materie. Een boek is materie, een computer is materie, voedsel is materie, en vuil in de grond is materie. Soms kan materie moeilijk te identificeren zijn. Lucht is bijvoorbeeld materie, maar omdat het zo dun is vergeleken met andere materie (bijvoorbeeld een boek, een computer, voedsel en vuil), vergeten we soms dat lucht massa heeft en ruimte inneemt. Dingen die geen materie zijn, zijn bijvoorbeeld gedachten, ideeën, emoties en hoop.
Voorbeeld 1
Welke van de volgende dingen is materie en geen materie?
- een hotdog
- liefde
- een boom
Oplossing
- Een hotdog heeft massa en neemt ruimte in beslag, dus is het materie.
- Liefde is een emotie, en emoties zijn geen materie.
- Een boom heeft massa en neemt ruimte in beslag, dus is het materie.
Test jezelf
Welk van de volgende dingen is materie en geen materie?
- de maan
- een idee voor een nieuwe uitvinding
Antwoord
- de maan is materie.
- De uitvinding zelf kan materie zijn, maar het idee ervoor niet.
Figuur 1.1 De fasen van materie

“IJsblokjes” door Darren Hester is gelicenseerd onder de Creative Commons Naamsvermelding-GelijkDelen 2.5 Generic; “Glas water” door Greg Riegler is gelicenseerd onder de Creative Commons Naamsvermelding 2.0 Generic; Tea Time door Vélocia is gelicenseerd onder de Creative Commons Naamsvermelding-NietCommercieel-GeenDerivs 2.0 Generic.
Om materie te begrijpen en hoe het verandert, moeten we in staat zijn om materie te beschrijven. Er zijn twee basismanieren om materie te beschrijven: fysische eigenschappen en chemische eigenschappen. Fysische eigenschappen zijn kenmerken die materie beschrijven zoals zij bestaat. Enkele van de vele fysische eigenschappen van materie zijn vorm, kleur, grootte en temperatuur. Een belangrijke fysische eigenschap is de fase (of toestand) van materie. De drie fundamentele fasen van materie zijn vast, vloeibaar en gas (zie figuur 1.1 “De fasen van materie”).
Figuur 1.2 Chemische eigenschappen
Het feit dat deze lucifer brandt is een chemische eigenschap van de lucifer.

“aansteken van een lucifer” (http://commons.wikimedia.org/wiki/File:Match_stick,_lit_a_match,_match_box,_fire.JPG) door Jith JR is gelicenseerd onder de Creative Commons Naamsvermelding-GelijkDelen 3.0 Ongeportioneerd.
Chemische eigenschappen zijn eigenschappen van materie die beschrijven hoe materie van vorm verandert in aanwezigheid van andere materie. Brandt een monster van materie? Verbranden is een chemische eigenschap. Gedraagt het zich gewelddadig als het in water wordt gedaan? Ook deze reactie is een chemische eigenschap (figuur 1.2 “Chemische eigenschappen”). In de volgende hoofdstukken zullen we zien hoe beschrijvingen van fysische en chemische eigenschappen belangrijke aspecten van de scheikunde zijn.
Figuur 1.3 Fysische veranderingen
Het vaste ijs smelt in vloeibaar water-een fysische verandering.

“Smeltende ijsblokjes” (https://www.flickr.com/photos/jariceiii/5012344135/) door Jar is gelicenseerd onder Creative Commons Attribution 2.0 Generic.
Als de materie altijd hetzelfde zou blijven, zou scheikunde nogal saai zijn. Gelukkig bestaat een groot deel van de scheikunde uit verandering. Een fysische verandering treedt op wanneer een stuk materie een of meer van zijn fysische eigenschappen verandert. Een vaste stof kan bijvoorbeeld smelten (figuur 1.3 “Fysische veranderingen”), of de alcohol in een thermometer kan van volume veranderen als de temperatuur verandert. Een fysische verandering heeft geen invloed op de chemische samenstelling van materie.
Een chemische verandering is het proces waarbij een chemische eigenschap wordt aangetoond, zoals de brandende lucifer in figuur 1.2 “Chemische eigenschappen”. Als de materie in de lucifer verbrandt, verandert de chemische samenstelling en ontstaan nieuwe vormen van materie met nieuwe fysische eigenschappen. Merk op dat chemische veranderingen vaak gepaard gaan met fysische veranderingen, omdat de nieuwe materie waarschijnlijk andere fysische eigenschappen zal hebben dan de oorspronkelijke materie.
Voorbeeld 2
Beschrijf elk proces als een fysische verandering of een chemische verandering.
- Water in de lucht verandert in sneeuw.
- Het haar van een persoon wordt geknipt.
- Brooddeeg wordt vers brood in een oven.
Oplossing
- Omdat het water van een gasfase naar een vaste fase gaat, is dit een fysische verandering.
- Jouw lange haar wordt korter gemaakt. Dit is een fysische verandering.
- Omdat de oven op temperatuur is, vinden er chemische veranderingen plaats in het brooddeeg om vers brood te maken. Dit zijn chemische veranderingen. (In feite gaat veel koken gepaard met chemische veranderingen.)
Test jezelf
Identificeer elk proces als een fysische verandering of een chemische verandering.
- Er woedt een vuur in een open haard.
- Water wordt verwarmd om een kopje koffie te zetten.
Antwoorden
- chemische verandering
- fysische verandering
Een monster van materie dat overal dezelfde fysische en chemische eigenschappen heeft, wordt een stof genoemd. Soms wordt de uitdrukking zuivere stof gebruikt, maar het woord zuiver is niet nodig. De definitie van de term stof is een voorbeeld van hoe de scheikunde een specifieke definitie heeft voor een woord dat in het dagelijks taalgebruik een andere, vagere definitie heeft. Hier zullen we de term stof gebruiken met zijn strikte chemische definitie.
De scheikunde kent twee verschillende soorten stoffen: elementen en verbindingen. Een element is het eenvoudigste type van chemische substantie; het kan niet met gewone chemische middelen in eenvoudiger chemische substanties worden opgesplitst. Er zijn ongeveer 115 elementen bekend in de wetenschap, waarvan er 80 stabiel zijn. (De andere elementen zijn radioactief, een toestand die we zullen behandelen in hoofdstuk 15 “Nucleaire chemie”). Elk element heeft zijn eigen unieke fysische en chemische eigenschappen. Voorbeelden van elementen zijn ijzer, koolstof en goud.
Een verbinding is een combinatie van meer dan één element. De fysische en chemische eigenschappen van een verbinding zijn verschillend van de fysische en chemische eigenschappen van de samenstellende elementen; dat wil zeggen dat de verbinding zich gedraagt als een geheel andere stof. Er zijn meer dan 50 miljoen verbindingen bekend, en dagelijks worden er nog meer ontdekt. Voorbeelden van verbindingen zijn water, penicilline, en natriumchloride (de chemische naam voor keukenzout).
Elementen en verbindingen zijn niet de enige manieren waarop materie aanwezig kan zijn. We komen vaak voorwerpen tegen die fysieke combinaties zijn van meer dan één element of verbinding. Fysische combinaties van meer dan één stof worden mengsels genoemd. Er zijn twee soorten mengsels. Een heterogeen mengsel is een mengsel dat bestaat uit twee of meer stoffen. Het is gemakkelijk te zien, soms met het blote oog, dat er meer dan één stof aanwezig is. Een homogeen mengsel is een combinatie van twee of meer stoffen die zo innig gemengd zijn dat het mengsel zich gedraagt als één enkele stof. Een ander woord voor een homogeen mengsel is oplossing. Zo is een combinatie van zout en staalwol een heterogeen mengsel, omdat gemakkelijk te zien is welke deeltjes van de stof zoutkristallen zijn en welke staalwol. Aan de andere kant, als je zoutkristallen neemt en ze oplost in water, is het heel moeilijk om te zien dat je meer dan één stof hebt door alleen maar te kijken – zelfs als je een krachtige microscoop gebruikt. Het zout opgelost in water is een homogeen mengsel, of een oplossing (figuur 1.4 “Soorten mengsels”).
Figuur 1.4 Soorten mengsels

Voorbeeld 3
Benoem de volgende combinaties als heterogene mengsels of homogene mengsels.
- Sodawater (Koolstofdioxide is opgelost in water.)
- een mengsel van ijzermetaalvijlsel en zwavelpoeder (Zowel ijzer als zwavel zijn elementen.)
Oplossing
- Omdat koolstofdioxide in water is opgelost, kunnen we uit het gedrag van zoutkristallen opgelost in water afleiden dat koolstofdioxide opgelost in water (ook) een homogeen mengsel is.
- Aannemend dat het ijzer en de zwavel gewoon met elkaar zijn vermengd, moet het gemakkelijk te zien zijn wat ijzer is en wat zwavel, dus dit is een heterogeen mengsel.
Test jezelf
Zijn de volgende combinaties homogene mengsels of heterogene mengsels?
- het menselijk lichaam
- een amalgaam, een combinatie van enkele andere metalen opgelost in een kleine hoeveelheid kwik
Antwoorden
- heterogeen mengsel
- homogeen mengsel
Er zijn nog andere descriptoren die we kunnen gebruiken om materie te beschrijven, vooral elementen. Gewoonlijk kunnen we elementen onderverdelen in metalen en niet-metalen, en elke groep heeft bepaalde (maar niet altijd alle) eigenschappen gemeen. Een metaal is een element dat vast is bij kamertemperatuur (hoewel kwik een bekende uitzondering is), glanzend en zilverachtig is, elektriciteit en warmte goed geleidt, in dunne platen kan worden geperst (een eigenschap die smeedbaarheid wordt genoemd), en in dunne draden kan worden getrokken (een eigenschap die vervormbaarheid wordt genoemd). Een niet-metaal is een element dat in vaste toestand bros is, elektriciteit of warmte niet goed geleidt, en niet tot dunne platen of draden kan worden gemaakt (figuur 1.5 “Semimetalen”). Niet-metalen bestaan ook in een verscheidenheid van fasen en kleuren bij kamertemperatuur. Sommige elementen hebben eigenschappen van zowel metalen als niet-metalen en worden halfmetalen (of metalloïden) genoemd. We zullen later zien hoe deze beschrijvingen vrij gemakkelijk aan verschillende elementen kunnen worden toegekend.
Figuur 1.5 Semimetalen

“Het gieten van vloeibaar kwik bionerd” is gelicenseerd onder de Creative CommonsAttribution 3.0 Unported; “Zwavel-vulkaan” door Heidi Soosalu is gelicenseerd onder de Creative Commons Attribution-Share Alike 3.0 Unported.
Figuur 1.6 “Materie beschrijven” is een stroomdiagram van de relaties tussen de verschillende manieren om materie te beschrijven.
Figuur 1.6 “Materie beschrijven” is een stroomdiagram van de relaties tussen de verschillende manieren om materie te beschrijven.
Figuur 1.6 “Materie beschrijven” is een stroomdiagram van de relaties tussen de verschillende manieren om materie te beschrijven.6 Materie beschrijven
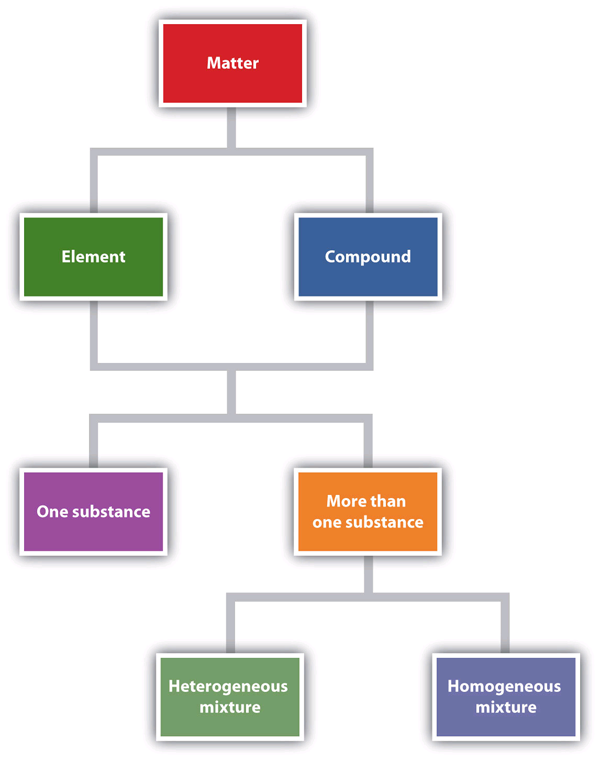
Dit stroomdiagram laat zien hoe materie kan worden beschreven.
Chemistry Is Everywhere: In the Morning
De meeste mensen hebben een ochtendritueel, een proces dat ze elke ochtend doorlopen om zich klaar te maken voor de dag. Bij veel van deze activiteiten komt chemie om de hoek kijken.
- Als je ’s ochtends een douche of bad neemt, gebruik je waarschijnlijk zeep, shampoo, of allebei. Deze producten bevatten chemicaliën die een wisselwerking aangaan met de olie en het vuil op uw lichaam en haar om deze te verwijderen en weg te wassen. Veel van deze producten bevatten ook chemicaliën die je lekker laten ruiken; ze worden geurstoffen genoemd.
- Wanneer je ’s ochtends je tanden poetst, gebruik je meestal tandpasta, een vorm van zeep, om je tanden schoon te maken. Tandpasta’s bevatten meestal kleine, harde deeltjes die schuurmiddelen worden genoemd en die uw tanden fysiek schuren. Veel tandpasta’s bevatten ook fluoride, een stof die een chemische interactie aangaat met het oppervlak van de tanden om gaatjes te helpen voorkomen.
- Misschien neemt u elke ochtend vitaminen, supplementen of medicijnen. Vitaminen en andere supplementen bevatten chemische stoffen die uw lichaam in kleine hoeveelheden nodig heeft om goed te functioneren. Medicijnen zijn chemische stoffen die helpen ziekten te bestrijden en de gezondheid te bevorderen.
- Misschien maakt u een paar gebakken eieren voor het ontbijt. Bij het bakken van eieren worden ze voldoende verhit, zodat er een chemische reactie optreedt om de eieren gaar te maken.
- Na het eten wordt het voedsel in de maag chemisch gereageerd, zodat het lichaam (meestal de darmen) voedsel, water en andere voedingsstoffen kan opnemen.
- Als u met de auto of de bus naar school of uw werk gaat, gebruikt u een voertuig dat waarschijnlijk benzine verbrandt, een materiaal dat vrij gemakkelijk brandt en energie levert om het voertuig aan te drijven. Denk eraan dat verbranding een chemische verandering is.
Dit zijn maar een paar voorbeelden van de invloed van chemie op je dagelijks leven. En we zijn nog niet eens aan de lunch toegekomen!
Figuur 1.7 Scheikunde in het dagelijks leven

“Soaps and Shampoos” door Takashi Ota is gelicenseerd onder Creative Commons Naamsvermelding 2.0 Generic; “English Breakfast” is gelicenseerd onder de Creative Commons Naamsvermelding-GelijkDelen 3.0 Unported; “Langley, Trans-Canada Highway” door James is gelicenseerd onder de Creative Commons Naamsvermelding-GelijkDelen 3.0 Unported.

Videobron: De chemische wereld door keyj (https://viuvideos.viu.ca/media/The+Chemical+World/0_ixlxmwe8)
Key Takeaways
- Chemie is de studie van materie en haar interacties met andere materie en energie.
- Materie is alles wat massa heeft en ruimte inneemt.
- Materie kan worden beschreven in termen van fysische eigenschappen en chemische eigenschappen.
- Fysische eigenschappen en chemische eigenschappen van materie kunnen veranderen.
- Materie is opgebouwd uit elementen en verbindingen.
- Combinaties van verschillende stoffen worden mengsels genoemd.
- Elementen kunnen worden beschreven als metalen, niet-metalen, en halfmetalen.
Oefeningen
- Identificeer elk als ofwel materie ofwel geen materie.
a) een boek
b) haat
c) licht
d) een auto
e) een gebakken ei
2. Geef een voorbeeld van materie in elke fase: vast, vloeibaar, of gas.
3. Staat elke uitspraak voor een fysische eigenschap of een chemische eigenschap?
a) Zwavel is geel.
b) Staalwol brandt als het aangestoken wordt door een vlam.
c) Een liter melk weegt meer dan acht pond.
4. Staat elke uitspraak voor een fysische eigenschap of een chemische eigenschap?
a) Een stapel bladeren rot langzaam weg in de achtertuin.
b) In aanwezigheid van zuurstof kan waterstof samenwerken om water te maken.
c) Goud kan worden uitgerekt tot zeer dunne draden.
5. Staat elke bewering voor een fysische verandering of een chemische verandering?
a) Water kookt en wordt stoom.
b) Voedsel wordt door het spijsverteringsstelsel omgezet in bruikbare vorm.
c) De alcohol in veel thermometers bevriest bij ongeveer -40 graden Fahrenheit.
6. Staat elke bewering voor een fysische verandering of een chemische verandering?
a) Grafiet, een vorm van elementaire koolstof, kan bij zeer hoge temperatuur en druk worden omgezet in diamant, een andere vorm van koolstof.
b) Het huis aan de overkant van de straat is in een nieuwe kleur geschilderd.
c) De elementen natrium en chloor komen samen om een nieuwe stof te maken die natriumchloride heet.
7. Maak onderscheid tussen een element en een verbinding. Hoeveel zijn er van elk bekend?
8. Wat is het verschil tussen een homogeen mengsel en een heterogeen mengsel?
9. Noem elk een heterogeen mengsel of een homogeen mengsel.
a) Zout wordt gemengd met peper.
b) Suiker wordt opgelost in water.
c) Pasta wordt gekookt in kokend water.
10. Identificeer elk als een heterogeen mengsel of een homogeen mengsel.
a) lucht
b) vuil
c) een televisietoestel
11. Welke keuzes in oefening 9 zijn ook oplossingen?
12. Welke keuzes zijn in opgave 10 ook oplossingen?
13. Waarom wordt ijzer beschouwd als een metaal?
14. Waarom wordt zuurstof beschouwd als een niet-metaal?
15. Maak een onderscheid tussen een metaal en een niet-metaal.
16. Welke eigenschappen hebben semimetalen?
17. Elementair koolstof is een zwarte, dof uitziende vaste stof die goed warmte en elektriciteit geleidt. Het is zeer bros en kan niet tot dunne platen of lange draden worden gemaakt. Van deze eigenschappen, hoe gedraagt koolstof zich als een metaal? Hoe gedraagt koolstof zich als niet-metaal?
18. Zuiver silicium is glanzend en zilverachtig, maar geleidt elektriciteit en warmte niet goed. Van deze eigenschappen, hoe gedraagt silicium zich als een metaal? Hoe gedraagt silicium zich als een niet-metaal?
Antwoorden
a) materie
b) geen materie
c) geen materie
d) materie
a) fysische eigenschap
b) chemische eigenschap
c) fysische eigenschap
a) fysische verandering
b) chemische verandering
c) fysische verandering
a) heterogeen
b) homogeen
c) heterogeen
11. Keuze b is een oplossing.
13. IJzer is een metaal omdat het vast is, glimt, en elektriciteit en warmte goed geleidt.
15. Metalen zijn meestal glanzend, geleiden elektriciteit en warmte goed, en zijn kneedbaar en buigzaam; niet-metalen hebben een verscheidenheid aan kleuren en fasen, zijn bros in de vaste fase, en geleiden warmte en elektriciteit niet goed.
17. Koolstof gedraagt zich als een metaal omdat het warmte en elektriciteit goed geleidt. Het is een niet-metaal omdat het zwart en bros is en niet tot platen of draden kan worden verwerkt.