Photoelektrischer Effekt
Albert Einstein zeigte, dass die Abhängigkeit von der Frequenz mit der klassischen Wellentheorie allein nicht zu rechtfertigen war, also lieferte er eine Teilchensicht. 1905 erklärte er, dass Photonen (von G.N. Lewis benannt), „Lichtteilchen“ sind, die eine ähnliche Energie haben, wie die Plancksche Gleichung. Diese Gleichung besagt, dass die Frequenz und die Energie eines Quants der elektromagnetischen Strahlung proportional sind. Einsteins Idee war revolutionär, weil er eine neue Perspektive einbrachte, Licht nicht nur als Welle, sondern als Teilchen zu betrachten.
Plancksche Gleichung: E=hv Plancksche Konstante: h=6,626×10-34 Js 
Das Phänomen des photoelektrischen Effekts, dass Elektronen emittiert werden, wenn Licht auf die Oberfläche von Metallen trifft, wurde 1888 von Heinrich Hertz entdeckt. Dieser Vorgang findet statt, wenn das einfallende Licht eine höhere Frequenz als einen bestimmten Schwellenwert hat. Die Menge der ausgestoßenen Elektronen wird durch die Intensität des einfallenden Lichts bestimmt, die Frequenz des Lichts wirkt sich jedoch auf die kinetischen Energien der emittierten Elektronen aus.
Mit anderen Worten kann die Intensität als die Helligkeit einer Lichtquelle beschrieben werden. Erhöht man also die Helligkeit, steigt die Intensität und damit auch die freigesetzte Energie. Die abgegebene Energie wird größer und wenn dies geschieht, vergrößert sich die Amplitude der Lichtwelle. Aber es spielt keine Rolle, wie viel Energie erhöht wird oder wie sehr man die Amplitude erhöht, wenn es darum geht, Elektronen aus einer metallischen Oberfläche zu emittieren. Dazu muss die Frequenz erhöht werden.
Erhöhen Sie die Helligkeit (behält die Frequenz und Energie bei)–>Erhöhen Sie die Intensität (erhöht die phot ons)–>Erhöht die Anzahl der emittierten Elektronen
ons)–>Erhöht die Anzahl der emittierten Elektronen
Erhöht die Frequenz–>Erhöht die kinetische Energie der Elektronen
Einstein erklärte, dass Licht die Eigenschaft eines Teilchens (Photon) mit der Photonenenergie von E=hv hat. Er schloss daraus, dass, wenn die Grenzfrequenz des Metalls größer ist als die Frequenz des Photons, das Photon keine Wirkung hat, wenn es die Metalloberfläche bombardiert. Wenn das Photon jedoch die Schwellenfrequenz erreichte, konnte es die Emission eines Elektrons bewirken. Um mehr Elektronen zu emittieren, muss die Lichtquelle aufgehellt werden, um die Intensität zu erhöhen, was immer noch die Frequenz des Lichts und die gleiche Energie beibehält, aber die Anzahl der Photonen erhöht.
Schwellenwertfrequenz: Vo= (eVo)/h = Arbeitsfunktion/Plancksche Konstante
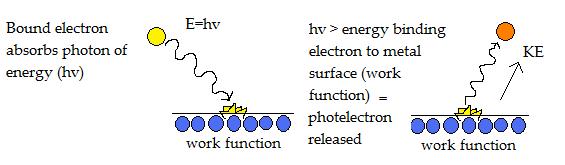
Der photoelektrische Effekt kann schon bei Licht mit der niedrigsten Frequenz, der sogenannten Schwellenfrequenz, auftreten.
Photelektronen werden freigesetzt, wenn die Photonenenergie (hv) größer als die Arbeitsfunktion ist. Die überschüssige Energie wird als kinetische Energie im ausgeworfenen Photoelektron freigesetzt und ist proportional zur Frequenz des Lichts.
Das obige Diagramm zeigt ein Elektron, das von einem Photon mit einer Energie getroffen wird, die es ihm erlaubt, die Arbeitsfunktion zu überwinden, die es an die Metalloberfläche bindet. Als Ergebnis wird ein Photoelektron mit kinetischer Energie emittiert.
Durch Anwendung des Energieerhaltungssatzes erhalten wir die Gleichung: hv =eVo+(1/2)mv2
Zusammenfassend lässt sich sagen, dass unabhängig von der Intensität des Lichts keine Elektronen emittiert werden, wenn die Frequenz des Lichts unterhalb der Schwellenfrequenz (Vo) der Metalloberfläche liegt.

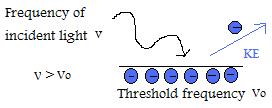
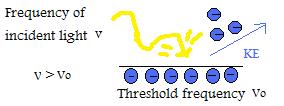
- Wenn die Frequenz des einfallenden Lichts oberhalb der Schwellenfrequenz liegt, dann steigt die kinetische Energie des emittierten Teilchens linear mit dem Betrag der Frequenz.
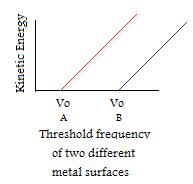
- Wenn die Frequenz des einfallenden Lichts größer als die Schwellenfrequenz ist, wird die Anzahl der emittierten Elektronen durch die Intensität bestimmt. (WICHTIGER HINWEIS: Die kinetische Energie pro Elektron ändert sich nicht, wenn die Intensität geändert wird, sondern nur, wenn die Frequenz manipuliert wird)
- Obwohl jedes Metall seine eigene einzigartige Schwellenfrequenz hat, weisen alle ähnliche Muster auf.