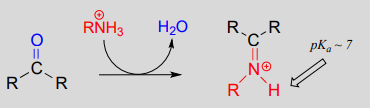
El átomo de carbono electrófilo de los aldehídos y las cetonas puede ser el objetivo del ataque nucleófilo de las aminas, así como de los alcoholes. El resultado final del ataque de un nucleófilo amina es un grupo funcional en el que el doble enlace C=O se sustituye por un doble enlace C=N, y se conoce como imina. (Un término equivalente es «base de Schiff», pero utilizaremos «imina» a lo largo de este libro). Recordemos de la sección 7.5B que las iminas tienen un pKa de aproximadamente 7, por lo que a pH fisiológico pueden dibujarse con precisión como protonadas (forma de ion iminio) o neutras (imina).
Formación del ion iminio:
Mecanismo (enzimático):
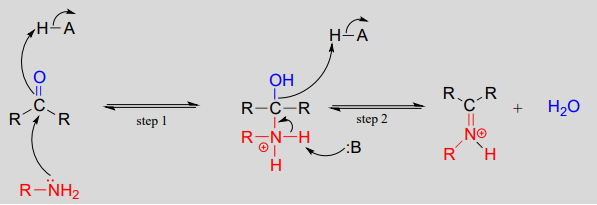
Mecánicamente, la formación de una imina implica dos pasos. Primero, el nitrógeno de la amina ataca al carbono del carbonilo en un paso de adición nucleofílica (paso 1) que es muy análogo a la formación de hemiacetales y hemiketales. Basándote en tu conocimiento del mecanismo de formación de acetales y cetales, podrías esperar que el siguiente paso fuera el ataque de una segunda amina para formar un compuesto con un carbono unido a dos grupos aminos – la versión nitrogenada de un cetal o acetal. En cambio, lo que ocurre a continuación (paso 2 anterior) es que los electrones del par solitario del nitrógeno «empujan» al oxígeno fuera del carbono, formando un doble enlace \(C=N\) (un iminio) y una molécula de agua desplazada.
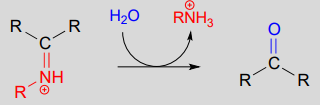
La conversión de un iminio de nuevo a un aldehído o cetona es un proceso hidrolítico (los enlaces se rompen por una molécula de agua), y mecánicamente es simplemente la inversa de la formación del iminioma:
Hidrólisis de un ion iminio:
Mecanismo (enzimático):
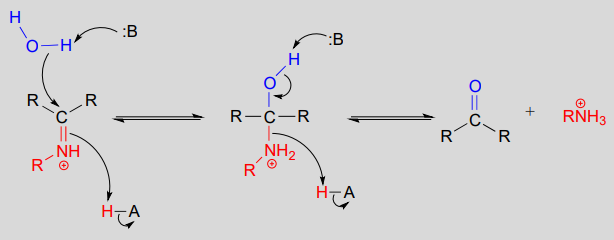
Las enzimas formadoras de enlaces carbono-carbono llamadas aldolasas (que veremos en detalle en el capítulo 12) suelen formar enlaces de iminio entre un carbono carbonilo de un sustrato y un residuo de lisina del sitio activo de la enzima, como en esta reacción de la aldolasa del Ciclo de Calvin:
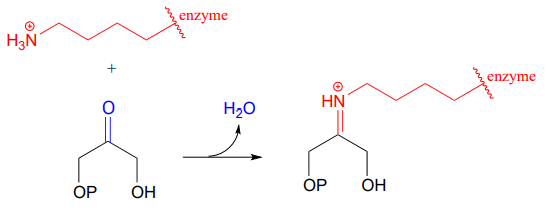
Después de que se complete el enlace carbono-carbono que forma parte de una reacción de aldolasa, el enlace de iminio se hidroliza, liberando el producto para que pueda difundirse fuera del sitio activo y permitir que comience otro ciclo catalítico.
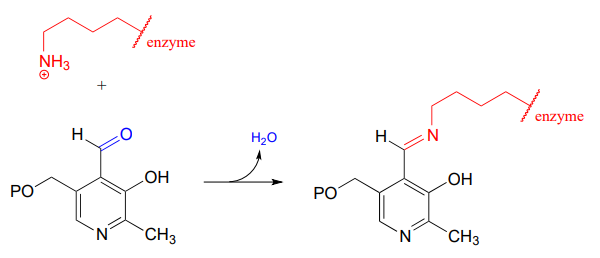
Entonces, el enlace de imina \(PLP\)-lisina se intercambia por un enlace de imina entre \(PLP\) y el grupo amino del sustrato, en lo que puede denominarse una transiminación.
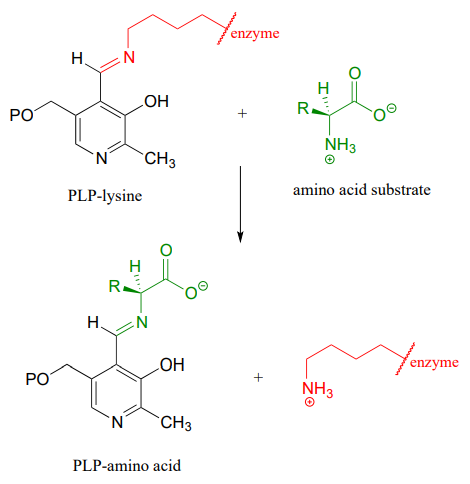
El mecanismo de una transiminación es muy similar al de la formación de iminas:
Reacción de transiminación:
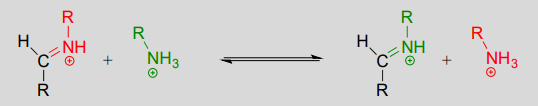
Mecanismo:
Ejercicio \N(\PageIndex{1})
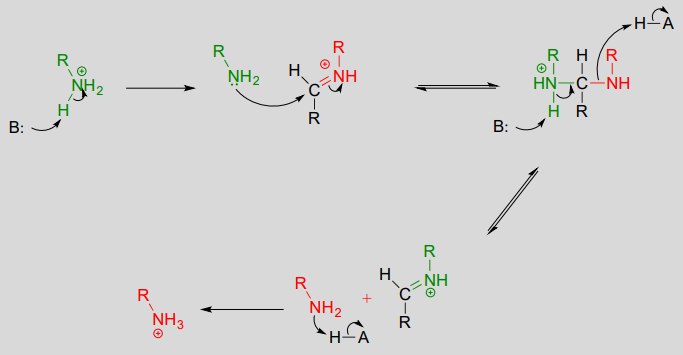
Dibuja una imina que podría formarse entre cada par de compuestos.
a.
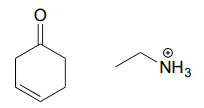
b.
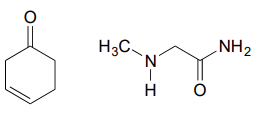
c.
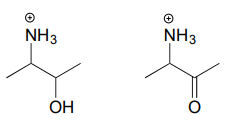
Ejercicio \N(\NPageIndex{2})
Dibuja el producto de hidrólisis del inminio para cada uno de los siguientes compuestos.
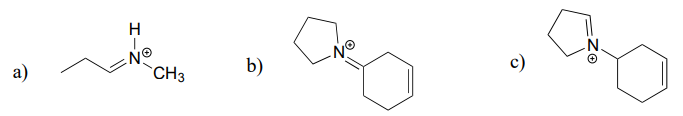
Agrega el texto de la respuesta aquí y se ocultará automáticamente si tienes una plantilla «AutoNum» activa en la página.
Ejercicio \N(\NPageIndex{3})
- El intermediario metabólico que se muestra a continuación sufre una formación intramolecular de imina como paso en la biosíntesis de la lisina (EC 4.3.3.7). Dibuja el producto de este paso de formación de imina intramolecular.
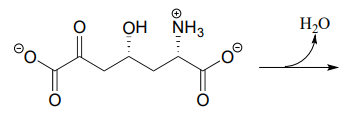
- Prediga el producto de este paso de hidrólisis de imina (EC 2.3.1.117) de la vía de degradación de la prolina.
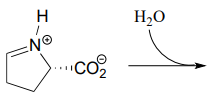
Contribuidores
-
Química orgánica con énfasis biológico por Tim Soderberg (Universidad de Minnesota, Morris)