Por Caroline Helwick
25 de mayo de 2019

En pacientes con mieloma múltiple smolder de riesgo intermedio a alto, el tratamiento con lenalidomida como agente único, frente a la observación, condujo a una reducción del 72% del riesgo de progresión de la enfermedad a los 3 años.1 Los resultados del estudio de fase III E3A06 fueron presentados en una rueda de prensa previa a la Reunión Anual de la ASCO de 2019 por Sagar Lonial, MD, FACP, de la Universidad de Emory, Atlanta.
«Demostramos, en el mayor estudio aleatorizado hasta la fecha en mieloma smoldering, que podemos prevenir el desarrollo de mieloma sintomático en una fracción significativa de pacientes», dijo el Dr. Lonial. Más del 90% del grupo de intervención permaneció libre de progresión a los 3 años, informó.

No sabemos si una verdadera estrategia de tratamiento marca la diferencia, pero hemos demostrado que la intervención puede marcarla.
– Sagar Lonial, MD, FACPTweet this quote
Aunque los pacientes con mieloma múltiple latente -una entidad temprana y asintomática que carece de la presencia de criterios CRAB (calcio elevado, insuficiencia renal, anemia, lesiones óseas)- suelen ser controlados y no tratados, algunos investigadores se han preguntado si una intervención temprana podría mejorar los resultados e incluso curar la enfermedad antes de que se sienta su impacto total.
«No hay duda de que los pacientes con mieloma múltiple necesitan un tratamiento inmediato para revertir las evidencias de daños en los órganos, pero un reto con el que hemos luchado es tratar de identificar a los pacientes sin daños en los órganos que tienen un mayor riesgo de progresión de la enfermedad, y tratar de intervenir», dijo el Dr. Lonial.
Los pacientes clasificados como con enfermedad latente generalmente tienen un riesgo de progresión de la enfermedad de alrededor del 10% por año. Después de 5 años, aproximadamente la mitad de estos pacientes tendrán enfermedad sintomática, dijo.
Entre los hallazgos anteriores del Grupo Español de Mieloma
El estudio se basa en un trabajo anterior del Grupo Español de Mieloma, que informó en el ensayo PETHEMA de 2015, más pequeño, de que lenalidomida/dexametasona mejoraba la supervivencia libre de progresión y global, frente a la observación, en pacientes con alto riesgo de progresión de la enfermedad.2
Ese estudio, sin embargo, fue criticado en aspectos que fueron evitados por el diseño del estudio actual: los pacientes no fueron examinados con técnicas de imagen avanzadas; los investigadores aplicaron una definición anticuada de alto riesgo; y el régimen incluyó dexametasona, lo que hizo imposible aislar el efecto de la lenalidomida, dijo.
«El hecho de que el estudio no utilizara imágenes modernas es importante, porque los pacientes con radiografías negativas pueden tener enfermedad ósea por resonancia magnética (RM) o tomografía por emisión de positrones (PET)», señaló el doctor Lonial. «En nuestro estudio, exigimos una IRM antes de entrar en el estudio para estar seguros de que no estábamos inscribiendo a pacientes que ya tenían mieloma, que era la principal crítica del ensayo español.»
E3A06 también eliminó la dexametasona, que puede suprimir o eliminar el clon maligno y producir una respuesta temporal, a diferencia de controlar el clon, como era el objetivo de utilizar lenalidomida como agente único, dijo.
El ensayo anterior, por lo tanto -aunque se considera importante- no cambió el estándar de atención, «pero ahora», dijo, «con el ensayo E3A06, en conjunto con el ensayo PETHEMA, muchos de nosotros argumentaríamos que la intervención temprana con una estrategia de prevención puede reducir el riesgo de conversión a mieloma sintomático.»
Detalles del E3A06
El E3A06 fue un ensayo intergrupal aleatorizado de fase III que probó el efecto de la lenalidomida como agente único en comparación con la observación en pacientes clasificados con mieloma latente de riesgo intermedio o alto. La elegibilidad requería un porcentaje de células plasmáticas ≥ 10% y una proporción anormal de cadenas ligeras libres en suero (< 0,26 o > 1,65).
En una fase inicial de rodaje de la fase II, 44 pacientes recibieron lenalidomida para demostrar su seguridad. En el ensayo de fase III, 182 pacientes fueron asignados aleatoriamente a lenalidomida (25 mg/día durante 21 de 28 días) o a observación. Las características basales fueron similares entre los dos brazos. La mediana de seguimiento fue de 71 meses en la fase II y de 28 meses en la fase III. El criterio de valoración principal fue la supervivencia sin progresión.
Reducción significativa del riesgo de progresión
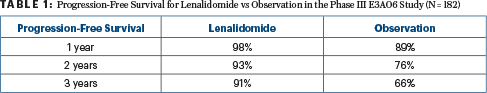
A los 3 años, el 87% de la cohorte de la fase II, todos los cuales recibieron lenalidomida, estaban libres de progresión, al igual que el 78% a los 5 años. En la comparación de la fase III, las tasas de supervivencia sin progresión a 1, 2 y 3 años fueron del 98%, 93% y 91% para la lenalidomida frente al 89%, 76% y 66%, respectivamente, para la observación (cociente de riesgos = 0,28; P = 0,0005), como se muestra en la Tabla 1. La tasa de respuesta global con lenalidomida fue del 47,7% en el estudio de fase II y del 48,9% en el de fase III, y no se observaron respuestas en el brazo de observación.
Es interesante que, cuando se desglosa en grupos de riesgo bajo, intermedio y alto, se observa que cada subconjunto se beneficia «casi por igual» de la intervención temprana. «Esto sugiere que, si bien los pacientes de alto riesgo pueden ser los que se dirigen ahora, un área fértil de investigación adicional puede ser el grupo intermedio, para el que ningún ensayo ha demostrado todavía un beneficio en la prevención de la enfermedad sintomática. Vemos un beneficio para los pacientes de riesgo intermedio, pero el seguimiento de la supervivencia global es demasiado corto para decir que todos estos pacientes deben ser tratados», concluyó.
Los pacientes de riesgo intermedio bajo se inscribieron cuando el estudio aflojó los criterios de elegibilidad para los ratios de cadenas ligeras libres ligeramente anormales. Aunque también obtuvieron beneficios, este no es un grupo a considerar para el tratamiento en este momento, añadió.
Eventos adversos
Se observaron toxicidades no hematológicas de grado 3 a 4 en aproximadamente el 28% de los pacientes, y toxicidad hematológica de grado 3 a 4 (principalmente neutropenia) en aproximadamente el 6%. La incidencia acumulada de neoplasias primarias invasivas fue del 5,2% para la lenalidomida y del 3,5% para la observación.
No hubo diferencias en las puntuaciones de calidad de vida entre los brazos. Sin embargo, el 80% de los pacientes de la fase II y el 51% de los de la fase III suspendieron la lenalidomida.
Mirando hacia el futuro
Es probable que una estrategia preventiva para el mieloma latente sea menos intensiva que las estrategias de tratamiento empleadas para la enfermedad sintomática, dijo. «Nos estamos centrando en mejorar la vigilancia inmunitaria del clon maligno existente y evitar que ese clon progrese, en lugar de erradicar la enfermedad, que es el objetivo del tratamiento», dijo el Dr. Lonial.
Los estudios en curso están, de hecho, persiguiendo intervenciones más agresivas, como la combinación de lenalidomida, dexametasona y daratumumab, u otros agentes activos nuevos. Otros estudios están evaluando el beneficio de la terapia de inducción, la consolidación, el trasplante y 2 años de mantenimiento en la enfermedad latente, dijo.
«No sabemos que una verdadera estrategia de tratamiento marque la diferencia, pero hemos demostrado que la intervención puede marcarla», dijo. «Ahora es el momento de explorar otras ideas, con regímenes más intensos y con un enfoque diferente». ■
DECLARACIÓN: El Dr. Lonial ha sido consultor o asesor de Celgene, Bristol-Myers Squibb, Janssen Oncology, Novartis, GlaxoSmithKline, Amgen, AbbVie, Takeda, Merck y Juno Therapeutics; y ha recibido financiación para investigaciones de Celgene, Bristol-Myers Squibb y Takeda.
1. Lonial S, Jacobus SJ, Weiss M, et al: E3A06: Ensayo aleatorizado de fase III de lenalidomida frente a observación sola en pacientes con mieloma múltiple asintomático de alto riesgo. Reunión anual de la ASCO 2019. Resumen 8001. Se presentará el 2 de junio de 2019.
2. Mateos M-V, Hernández M-T, Giraldo P, et al: Lenalidomida más dexametasona para el mieloma múltiple smoldering de alto riesgo. N Engl J Med 369:438-447, 2013.