Istnieją dwa podstawowe typy badań kohortowych oparte na tym, kiedy i w jaki sposób uczestnicy są włączani do badania:
Prospektywne badania kohortowe:
W prospektywnych badaniach kohortowych badacze wymyślają i projektują badanie, rekrutują uczestników i zbierają dane o ekspozycji wyjściowej wszystkich uczestników, zanim u któregokolwiek z nich rozwinął się jakikolwiek z interesujących go wyników. Uczestnicy są następnie śledzeni w przyszłości w celu zarejestrowania rozwoju któregokolwiek z interesujących ich wyników. Obserwacja może być prowadzona za pomocą kwestionariuszy pocztowych, wywiadów telefonicznych, przez Internet lub osobiście z wywiadami, badaniami fizycznymi i badaniami laboratoryjnymi lub obrazowymi. Można również stosować kombinacje tych metod.
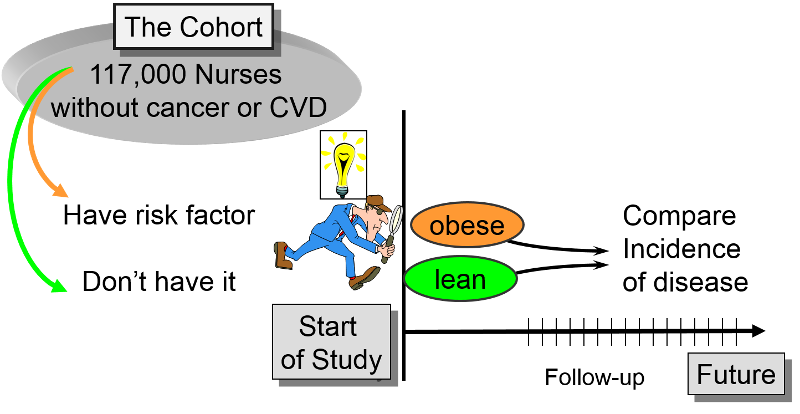
Typowo, badacze mają główny cel, na przykład, aby dowiedzieć się więcej o chorobach układu krążenia lub raku, ale dane zebrane z kohorty w czasie mogą być wykorzystane do odpowiedzi na wiele pytań i przetestowania wielu możliwych czynników, nawet tych, których nie brali pod uwagę, kiedy badanie było pierwotnie zaplanowane.
Badania Framingham Heart Study, Nurses Health Study i Black Women’s Health Study są dobrymi przykładami dużych, produktywnych prospektywnych badań kohortowych. W każdym z tych badań badaczom chodziło o zbadanie czynników ryzyka powszechnych chorób przewlekłych. Badacze zidentyfikowali kohortę (grupę) potencjalnych uczestników, których można by śledzić przez dłuższy czas. Kwalifikujący się uczestnicy musieli spełniać określone kryteria (kryteria włączenia), aby mogli zostać włączeni do badania jako uczestnicy. Następnie badacze określają początkową lub „wyjściową” charakterystykę, zachowania i inne „ekspozycje” wszystkich uczestników na początku badania. Informacje są zbierane od wszystkich uczestników w ten sam sposób, przy użyciu dokładnie tych samych pytań i metod zbierania danych dla wszystkich uczestników. Pytania i procedury zbierania danych są opracowywane bardzo starannie w celu uzyskania dokładnych informacji o narażeniu, zanim u któregoś z uczestników rozwinie się choroba.
Więcej informacji:
Link do Framingham Heart Study
Link do The Nurses Health Study
Link do The Black Women’s Health Study
Oczywiście analiza danych nie może mieć miejsca, dopóki nie wystąpi wystarczająca liczba „zdarzeń” lub „wyników”, więc musi upłynąć czas, a analizy będą dotyczyły zdarzeń, które wystąpiły w okresie od początku badania do czasu analizy lub zakończenia badania. Oczywiste jest, że analizy zawsze przeprowadza się retrospektywnie, ponieważ musi upłynąć pewien okres czasu, aby można było porównać częstość występowania. Tym, co czyni prospektywne badania kohortowe prospektywnymi, jest fakt, że zostały one zaprojektowane prospektywnie, a badani zostali włączeni do badania i mieli zebrane dane wyjściowe, zanim u któregokolwiek z nich wystąpił którykolwiek z interesujących nas wyników. Określenie stanu wyjściowego ekspozycji przed wystąpieniem zdarzeń chorobowych daje badaniom prospektywnym istotną przewagę w ograniczaniu pewnych rodzajów błędów, które mogą wystąpić w retrospektywnych badaniach kohortowych i badaniach case-control, choć kosztem efektywności.
Po zebraniu informacji wyjściowych, uczestnicy prospektywnego badania kohortowego są następnie śledzeni „wzdłuż”, tzn. przez pewien okres czasu, zwykle przez lata. Dzięki temu badacze wiedzą, kiedy rozpoczęła się obserwacja, czy i kiedy uczestnicy zachorowali, czy i kiedy utracili kontakt z badanym oraz czy ich status narażenia zmienił się w okresie obserwacji. Posiadając indywidualne dane dotyczące tych szczegółów dla każdego uczestnika, badacze mogą obliczyć i porównać współczynniki zachorowalności dla każdej z grup narażenia.
dla każdej z grup narażenia.
Lustracja poniżej przedstawia hipotetyczną grupę 12 uczestników, których obserwowano przez kilka lat. Zostali oni włączeni do badania w różnym czasie, a niektórzy z nich zaginęli, tzn. przestali odpowiadać na listy, e-maile i telefony, więc nie wiemy, co się z nimi stało; są oni przedstawieni za pomocą poziomej linii follow up zatrzymującej się.

Trzech badanych rozwinęło interesujący ich wynik w przybliżonych datach oznaczonych literami „X”. Częstość występowania została obliczona poprzez obliczenie czasu obserwacji wolnego od choroby dla każdego uczestnika, zsumowanie czasów obserwacji wolnych od choroby dla całej grupy, a następnie podzielenie tego na liczbę zdarzeń, jak pokazano w obliczeniach poniżej linii czasu.
Ponieważ badacze pytali o wiele narażeń podczas zbierania danych wyjściowych, mogą oni ostatecznie wykorzystać te dane do badania wielu związków pomiędzy różnymi narażeniami a wynikami choroby. Na przykład, można by zidentyfikować osoby palące i niepalące na linii podstawowej i porównać ich późniejszą częstość występowania chorób serca. Alternatywnie, można by pogrupować badanych na podstawie ich wskaźnika masy ciała (BMI) i porównać ich ryzyko rozwoju choroby serca lub raka.
Dane w poniższej tabeli podsumowują niektóre z wyników badania pochodzą z Nurses' Health Study, w którym badano związek wskaźnika masy ciała (BMI) z chorobą serca. (Link do artykułu)
pochodzą z Nurses' Health Study, w którym badano związek wskaźnika masy ciała (BMI) z chorobą serca. (Link do artykułu)
|
Wskaźnik masy ciała |
# Non-.śmiertelnych zawałów serca |
Osoba-rok obserwacji |
MI Rate per 100,000 osobo-latYears |
Rate Ratio |
|
<21 |
41 |
177,356 |
23.1 |
1.0 |
|
21-.23 |
57 |
194,243 |
29.3 |
1.3 |
|
23-.25 |
56 |
155,717 |
36.0 |
1.6 |
|
25-.29 |
67 |
148,541 |
45.1 |
2.0 |
|
>29 |
85 |
99,573 |
85.4 |
3.7 |
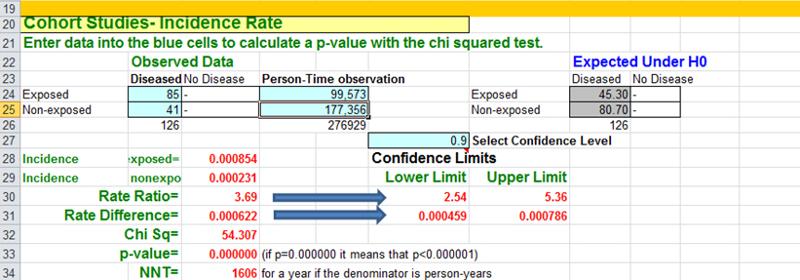
W badaniu wzięło udział ponad 118 000 pielęgniarek, a kohortę podzielono na pięć grup narażenia na podstawie BMI. W tym przypadku użyli wskaźnika zapadalności na zawały serca (MI, tj. ataki serca) u najchudszych kobiet (BMI < 21) jako odniesienia, z którym porównali wskaźniki zapadalności na MI w pozostałych czterech grupach. Na przykład, wskaźnik zapadalności na MI w grupie referencyjnej (osoby z BMI < 21) wynosił 23,1 na 100 000 osobo-lat obserwacji wolnej od choroby. Wskaźnik zachorowalności w grupie najcięższej (BMI > 29) wynosił 85,4 MI na 100 000 osobolat.
W arkuszu Epi-Tools.XLS dla badań kohortowych można porównywać zarówno skumulowaną zachorowalność (górna część arkusza), jak i wskaźniki zachorowalności takie jak te (dolna część arkusza). Na przykład, gdyby porównać grupę najcięższą (BMI > 29) do kobiet z BMI < 21 (grupa referencyjna), analiza Epi-Tools wyglądałaby następująco
Manson i wsp. wykorzystali również badanie Nurses' Health Study (NHS) do zbadania wpływu ćwiczeń fizycznych na choroby układu krążenia. Do NHS w 1976 roku zapisano 121 700 kobiet z RN, ale informacje o ćwiczeniach zaczęto zbierać dopiero w 1986 roku. Ponieważ pierwotne dane wyjściowe nie zawierały informacji o ćwiczeniach, w badaniu wykorzystano tylko te kobiety, u których do 1986 roku nie wystąpiły jeszcze żadne problemy sercowo-naczyniowe. Tak więc badanie dotyczące ćwiczeń fizycznych ograniczono do 72 448 osób, które w 1986 roku były wolne od chorób sercowo-naczyniowych i raka. W zasadzie informacje o ćwiczeniach i aktywności fizycznej, które zaczęto zbierać w 1986 roku, stanowiły nową linię odniesienia dla tego podzbioru oryginalnej kohorty.
wykorzystali również badanie Nurses' Health Study (NHS) do zbadania wpływu ćwiczeń fizycznych na choroby układu krążenia. Do NHS w 1976 roku zapisano 121 700 kobiet z RN, ale informacje o ćwiczeniach zaczęto zbierać dopiero w 1986 roku. Ponieważ pierwotne dane wyjściowe nie zawierały informacji o ćwiczeniach, w badaniu wykorzystano tylko te kobiety, u których do 1986 roku nie wystąpiły jeszcze żadne problemy sercowo-naczyniowe. Tak więc badanie dotyczące ćwiczeń fizycznych ograniczono do 72 448 osób, które w 1986 roku były wolne od chorób sercowo-naczyniowych i raka. W zasadzie informacje o ćwiczeniach i aktywności fizycznej, które zaczęto zbierać w 1986 roku, stanowiły nową linię odniesienia dla tego podzbioru oryginalnej kohorty.
Link do artykułu Mansona i wsp.
Retrospektywne badania kohortowe
Badania retrospektywne również grupują uczestników na podstawie ich statusu narażenia i porównują częstość występowania choroby. Jednak w tym przypadku zarówno status narażenia, jak i wynik są ustalane retrospektywnie.
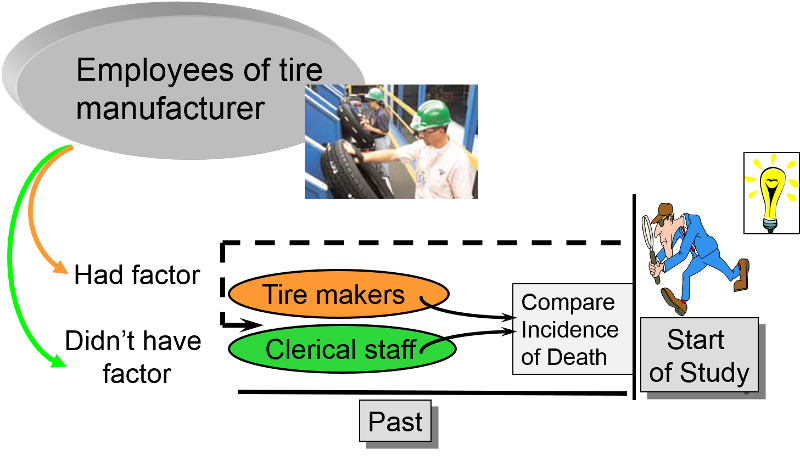
W zasadzie badacze cofają się w czasie, aby zidentyfikować użyteczną kohortę, która początkowo była wolna od choroby i „zagrożona”. Następnie używają wszelkich dostępnych zapisów, aby określić status ekspozycji każdego uczestnika na początku okresu obserwacji, a następnie ustalają, co później stało się z uczestnikami w dwóch (lub więcej) grupach ekspozycji. Retrospektywne badania kohortowe są również „podłużne”, ponieważ badają wyniki zdrowotne na przestrzeni czasu. Różnica polega na tym, że w retrospektywnych badaniach kohortowych wszystkie przypadki zachorowań wystąpiły już przed rozpoczęciem badania przez badaczy. W przeciwieństwie do tego, informacje o narażeniu są zbierane na początku prospektywnych badań kohortowych, zanim u jakiejkolwiek osoby rozwinął się którykolwiek z interesujących ją wyników, a okres „ryzyka” rozpoczyna się po zebraniu danych o narażeniu podstawowym i rozciąga się na przyszłość.
i „zagrożona”. Następnie używają wszelkich dostępnych zapisów, aby określić status ekspozycji każdego uczestnika na początku okresu obserwacji, a następnie ustalają, co później stało się z uczestnikami w dwóch (lub więcej) grupach ekspozycji. Retrospektywne badania kohortowe są również „podłużne”, ponieważ badają wyniki zdrowotne na przestrzeni czasu. Różnica polega na tym, że w retrospektywnych badaniach kohortowych wszystkie przypadki zachorowań wystąpiły już przed rozpoczęciem badania przez badaczy. W przeciwieństwie do tego, informacje o narażeniu są zbierane na początku prospektywnych badań kohortowych, zanim u jakiejkolwiek osoby rozwinął się którykolwiek z interesujących ją wyników, a okres „ryzyka” rozpoczyna się po zebraniu danych o narażeniu podstawowym i rozciąga się na przyszłość.
Retrospektywne badania kohortowe są szczególnie przydatne w przypadku nietypowych narażeń lub narażeń zawodowych. Na przykład, jeśli badacz chciałby ustalić, czy narażenie na substancje chemiczne stosowane w produkcji opon było związane ze zwiększonym ryzykiem zgonu, mógłby znaleźć fabrykę produkującą opony, która działała przez kilka dekad. Można by wykorzystać dokumentację zdrowotną pracowników, aby zidentyfikować tych, którzy wykonywali pracę wymagającą kontaktu z omawianymi substancjami chemicznymi (np. pracownicy, którzy faktycznie produkowali opony) oraz współpracowników, którzy nie byli narażeni na kontakt z tymi substancjami (np. pracownicy biurowi lub sprzedawcy w tej samej firmie lub, jeszcze lepiej, pracownicy również zaangażowani w działalność produkcyjną, ale wykonujący pracę, która nie wymagała kontaktu z tymi substancjami chemicznymi). Można by wówczas ustalić, co stało się ze wszystkimi badanymi i porównać częstość występowania zgonów u pracowników narażonych i nienarażonych.
Retrospektywne badania kohortowe tego typu są bardzo wydajne, ponieważ zajmują znacznie mniej czasu i kosztują znacznie mniej niż prospektywne badania kohortowe, ale ta zaleta stwarza również potencjalne problemy. Czasami status narażenia nie jest jasny, kiedy trzeba cofnąć się w czasie i wykorzystać wszelkie dostępne dane, ponieważ używane dane nie zostały zaprojektowane do wykorzystania w badaniu. Nawet gdyby było jasne, kto był narażony na działanie substancji chemicznych stosowanych przy produkcji opon na podstawie dokumentacji pracowniczej, ważne byłoby również uwzględnienie (lub skorygowanie) innych różnic, które mogły mieć wpływ na śmiertelność (czynniki zakłócające). Na przykład w badaniu porównującym śmiertelność wśród pracowników narażonych na rozpuszczalniki stosowane w produkcji opon i w grupie porównawczej, która nie była narażona, ważne może być dostosowanie czynników zakłócających, takich jak palenie tytoniu i spożywanie alkoholu. Jednakże jest mało prawdopodobne, aby retrospektywne badanie kohortowe posiadało dokładne informacje na temat tych innych czynników ryzyka.
Gdy w Milton w stanie MA wystąpił wybuch epidemii Giardia (patrz link do strony CDC na temat Giardia), Departament Zdrowia Milton poprosił o pomoc epidemiologów z Departamentu Zdrowia Publicznego w MA. (Kathleen MacVarish z Biura Praktyki BUSPH była agentem zdrowia w Milton, który prowadził dochodzenie). Prośba o pomoc została wystosowana jakiś czas po rozpoczęciu epidemii, a epidemia wygasała w czasie, gdy DPH rozpoczął swoje badania. Ognisko było wyraźnie skoncentrowane wśród członków Wollaston Golf Club w Milton, MA , który miał dwa baseny, jeden dla dorosłych i brodzik dla niemowląt i małych dzieci. Biorąc pod uwagę to, co wiedzieli o typowych mechanizmach przenoszenia Giardia, badacze uznali, że najbardziej prawdopodobnym źródłem było zanieczyszczenie basenu dla dzieci przez dziecko wydalające Giardia w swoim stolcu. (UWAGA
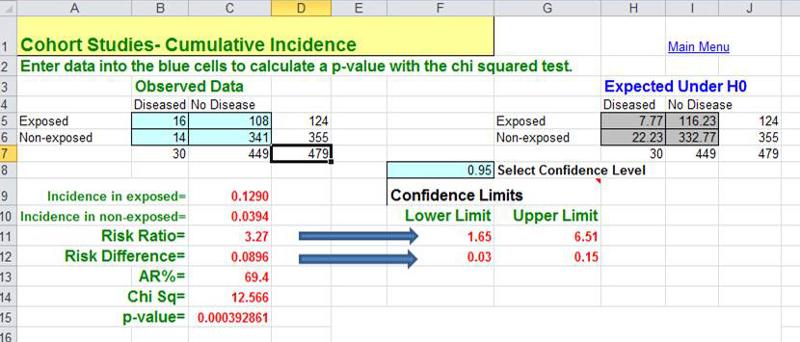
(patrz link do strony CDC na temat Giardia), Departament Zdrowia Milton poprosił o pomoc epidemiologów z Departamentu Zdrowia Publicznego w MA. (Kathleen MacVarish z Biura Praktyki BUSPH była agentem zdrowia w Milton, który prowadził dochodzenie). Prośba o pomoc została wystosowana jakiś czas po rozpoczęciu epidemii, a epidemia wygasała w czasie, gdy DPH rozpoczął swoje badania. Ognisko było wyraźnie skoncentrowane wśród członków Wollaston Golf Club w Milton, MA , który miał dwa baseny, jeden dla dorosłych i brodzik dla niemowląt i małych dzieci. Biorąc pod uwagę to, co wiedzieli o typowych mechanizmach przenoszenia Giardia, badacze uznali, że najbardziej prawdopodobnym źródłem było zanieczyszczenie basenu dla dzieci przez dziecko wydalające Giardia w swoim stolcu. (UWAGA ) Badanie zostało przeprowadzone poprzez nakłonienie większości osób z kohorty do wypełnienia kwestionariusza, w którym jedno z kluczowych pytań brzmiało „Czy spędziłeś jakikolwiek czas w basenie dla dzieci?”. Ta epidemia wyraźnie miała miejsce w dobrze zdefiniowanej kohorcie (członkowie klubu), a badacze mogli określić, u ilu osób rozwinęła się Giardia w każdej z grup narażenia (tj. narażonych na kontakt z basenem dla dzieci lub nie). Ponadto wiedzieli również, ilu respondentów było narażonych na kontakt z basenem dziecięcym, a ilu nie. Innymi słowy, znali mianowniki dla grup ekspozycji, więc mogli obliczyć skumulowaną częstość występowania, różnicę ryzyka i współczynnik ryzyka. Stwierdzili, że ludzie, którzy spędzali czas w basenie dla dzieci mieli o 9,0 przypadków na 100 osób więcej niż ci, którzy spędzali czas w basenie dla dzieci. Współczynnik ryzyka wynosił 3,27. Ponieważ dochodzenie rozpoczęło się już po wystąpieniu przypadków, badanie DPH dotyczące Giardia w Milton jest przykładem retrospektywnego badania kohortowego.
) Badanie zostało przeprowadzone poprzez nakłonienie większości osób z kohorty do wypełnienia kwestionariusza, w którym jedno z kluczowych pytań brzmiało „Czy spędziłeś jakikolwiek czas w basenie dla dzieci?”. Ta epidemia wyraźnie miała miejsce w dobrze zdefiniowanej kohorcie (członkowie klubu), a badacze mogli określić, u ilu osób rozwinęła się Giardia w każdej z grup narażenia (tj. narażonych na kontakt z basenem dla dzieci lub nie). Ponadto wiedzieli również, ilu respondentów było narażonych na kontakt z basenem dziecięcym, a ilu nie. Innymi słowy, znali mianowniki dla grup ekspozycji, więc mogli obliczyć skumulowaną częstość występowania, różnicę ryzyka i współczynnik ryzyka. Stwierdzili, że ludzie, którzy spędzali czas w basenie dla dzieci mieli o 9,0 przypadków na 100 osób więcej niż ci, którzy spędzali czas w basenie dla dzieci. Współczynnik ryzyka wynosił 3,27. Ponieważ dochodzenie rozpoczęło się już po wystąpieniu przypadków, badanie DPH dotyczące Giardia w Milton jest przykładem retrospektywnego badania kohortowego.
An Ambidirectional Cohort Study
Badanie kohortowe może być również ambidirectional , co oznacza, że istnieją zarówno retrospektywne jak i prospektywne fazy badania. Badania ambiwalentne są znacznie mniej powszechne niż badania czysto prospektywne lub retrospektywne, ale są one spójne koncepcyjnie i dzielą elementy zalet i wad obu typów badań. Badanie Air Force Health Study (AFHS) – znane również jako Ranch Hand Study – zostało zainicjowane przez Siły Powietrzne Stanów Zjednoczonych w 1979 roku w celu oceny możliwych skutków zdrowotnych narażenia personelu wojskowego na Agent Orange i inne defolianty rozpylane w czasie wojny w Wietnamie. Badanie przeprowadzono porównując:
- 1,098 pilotów narażonych na dioksyny w Wietnamie (Operacja Ranch Hand)
- 1,549 mężczyzn, którzy latali na misjach cargo w Azji Południowo-Wschodniej w tym samym czasie
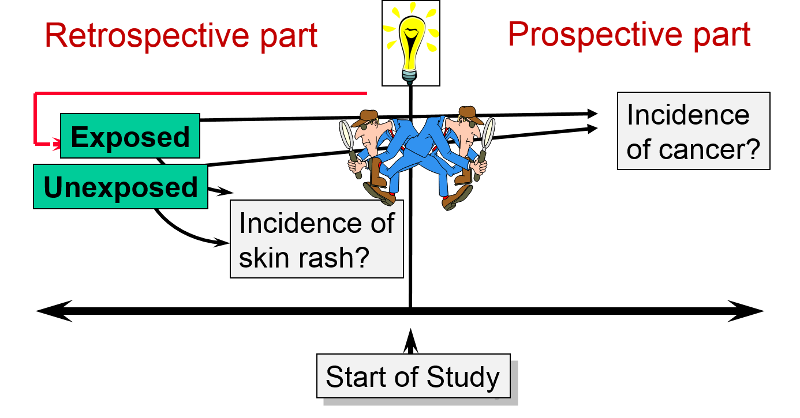
Jest to badanie „dwukierunkowe”, ponieważ miało zarówno komponent retrospektywny, jak i prospektywny. Niektóre z problemów podejrzewanych o spowodowanie przez Agent Orange wystąpiłyby wkrótce po ekspozycji (np. wysypki skórne). Zostały one uwzględnione poprzez retrospektywne spojrzenie na kohortę, aby sprawdzić, czy narażeni piloci mieli więcej problemów niż osoby z grupy kontrolnej. Inne problemy (np. niepłodność & rak) mogą nie pojawić się aż do pewnego czasu po ekspozycji. Dlatego kohorta była śledzona prospektywnie, aby zobaczyć, czy mieli większą częstość występowania tych problemów. Raporty, które pojawiły się w wyniku badań sugerowały powiązania między ekspozycją na Agent Orange a dziewięcioma różnymi chorobami: trądzikiem chlorkowym, chorobą Hodgkina, szpiczakiem mnogim, chłoniakiem nieziarniczym, porfirią skórną tardy, nowotworami układu oddechowego (płuc, oskrzeli, krtani i tchawicy), mięsakiem tkanek miękkich, ostrą i podostrą neuropatią obwodową oraz rakiem prostaty.
Kohorty zamknięte (stałe) kontra kohorty otwarte
Kohorta zamknięta to taka, w której liczba członków jest stała. Po zdefiniowaniu kohorty poprzez rekrutację uczestników i rozpoczęciu obserwacji, nikt nie może być dodany. Liczba uczestników może się zmniejszyć z powodu zgonu lub utraty follow up, ale nie dodaje się dodatkowych uczestników. W rezultacie zamknięte kohorty zawsze zmniejszają się z czasem. Obywatele Japonii, którzy byli narażeni na promieniowanie, kiedy bomby atomowe zostały zrzucone na Hiroszimę i Nagasaki podczas drugiej wojny światowej, byliby uważani za członków stałej lub zamkniętej kohorty, która została zdefiniowana przez wydarzenie. Ashengrau i Seage sklasyfikowaliby ofiary bombardowań jako „stałą kohortę” i dokonali rozróżnienia pomiędzy stałą kohortą a zamkniętą kohortą. Definiują oni zamkniętą kohortę jako podobną do stałej kohorty, z wyjątkiem tego, że zamknięta kohorta to taka, która nie ma strat, które można śledzić, na przykład kohorta osób, które uczestniczyły w obiedzie, który spowodował wybuch epidemii salmonellozy.
W przeciwieństwie do tego, otwarta kohorta jest dynamiczna, co oznacza, że członkowie mogą odejść lub zostać dodani w czasie. Rothman podaje przykład państwowego rejestru nowotworów. Osoby badane są stale dodawane, gdy zdiagnozowano u nich raka, więc nowe osoby są stale dodawane. Uczestnicy mogą również opuścić kohortę, przenosząc się do nowego stanu lub umierając. Innym przykładem otwartej lub dynamicznej kohorty byliby studenci Uniwersytetu Bostońskiego.
Te opisy powinny brzmieć znajomo, ponieważ są one zasadniczo równoległe do opisów stałych i dynamicznych populacji z modułu Miary częstości chorób. Większość badań kohortowych jest prowadzona w zamkniętych (lub stałych) kohortach, ponieważ trudniej jest ustalić kwalifikowalność i śledzić ludzi w otwartej kohorcie, ponieważ mogą oni wejść i wyjść w dowolnym momencie. Problem ten staje się coraz większy, gdy wielkość kohorty jest większa i/lub badanie trwa przez dłuższy czas. Zauważ, że retrospektywne badanie kohortowe Giardia w Milton było kohortą otwartą (członkowie klubu golfowego), ale populacja była stosunkowo mała, a okres czasu bardzo krótki.
powrót do góry | poprzednia strona | następna strona