INTRODUCTION
Human papilloma viruses (HPV) conform a heterogeneous viral group; their genome is constituted by a helicoidal double stranded DNA molecule with a protein capsid. Tworzą one jednostki epiteliotropowe, które zakażają nabłonek w stanie podstawowym i w rezultacie zachowują transkrypcję i replikację DNA na poziomie podstawowym, wytwarzając hiperplastyczne zmiany brodawczakowate i brodawkujące w skórze i błonach śluzowych.1
Istnieje ponad 230 typów HPV (118 z nich dobrze scharakteryzowanych) i ponad 40 typów analno-genitalnych, z których 15 jest onkogennych. U ludzi stanowią one jedną z grup wirusów częściej zakażających nabłonek skóry i błon śluzowych spojówek, jamy ustnej (genotypy 33 i 32) krtani, drzewa oskrzelowego, przełyku, pęcherza moczowego, odbytu i dróg rodnych.2,3
W przypadku HPV języka wyróżnia się dwie główne grupy obrazu klinicznego:
a) zmiany łagodne oraz b) zmiany przedzłośliwe lub złośliwe. Wśród łagodnych zmian w jamie ustnej można wyróżnić brodawczaka zwykłego, brodawczaka pospolitego, kłykciny kończyste jamy ustnej i ogniskową hiperplazję nabłonka (choroba Heckesa).4-6 Zmiany złośliwe i przedzłośliwe są reprezentowane głównie przez leukoplakię i raka płaskonabłonkowego.7
Brodawczak płaskonabłonkowy błony śluzowej jamy ustnej jest najczęściej stwierdzaną zmianą brodawkowatą, stanowi 2,5% lub wszystkie zmiany stwierdzane w jamie ustnej.6 Zmiany kliniczne HPV najczęściej obserwuje się na wardze górnej, wardze dolnej, wędzidełku językowym, grzbiecie języka i w kącikach warg.8
Najczęściej obserwowana morfologia tych zmian przybiera kształt kalafiorowaty, niemniej jednak można zaobserwować inne kształty, takie jak brodawki zwykłe, hiperkeratoza, a nawet powierzchnie nierogowaciejące, które wykazują powierzchowne zmiany koloru (zwykle fioletowy odcień).9 Według danych bibliograficznych choroba ta jest najczęściej przenoszona poprzez oralno-genitalne praktyki seksualne.10
Celem niniejszej pracy było dokonanie przeglądu piśmiennictwa dotyczącego brodawczaków jamy ustnej oraz przedstawienie przypadku klinicznego.
HISTOLOGIA JĘZYKA
Komórki znajdujące się w języku wykazują polistratyfikowany układ strukturalny. Osadzone są na (powierzchownej) warstwie rogowej, warstwie ziarnistej, kolczystej i podstawnej (warstwa najgłębsza). Jądro tych komórek zmienia swoją wielkość w zależności od ich dojrzałości i specjalizacji.11
GENOM WIRUSA PAPILOMA
Cząstki wirusowe zbudowane są z białkowego kapsydu, który składa się w 95% z białka L1 i w 5% z białka L2. Białka te łączą się ze sobą tworząc kapsomery o kształcie ikozahedralnym. Wewnątrz kapsydów znajduje się dwuniciowy kolisty DNA o długości około 8000 par zasad. Jest on utworzony przez osiem genów i nieskodyfikowany region regulatorowy; region ten zawiera miejsca łączenia dla czynników hormonalnych i białkowych gospodarza, potrzebnych wirusowi do zakończenia cyklu replikacyjnego.12
WirusHPV jest podobnie zbudowany przez dwa rodzaje genów: geny kodowane podczas wczesnych etapów zakażenia, lepiej znane jako geny E (E jak early) oraz geny kodowane podczas późnych etapów replikacji znane jako: E1, E2, E4, E5, E6, E7 (choć E4 jest uważany za gen późny), a także dwa geny późne, L1 i L2. Wczesne geny kodują białka zaangażowane w replikację i regulację wirusa, a także w jego zdolności rakotwórcze. Z drugiej strony, geny późne kodują białka strukturalne, które tworzą kapsyd wirusowy.12,13
CYKL ŻYCIA
HPV dostaje się do gospodarza przez małe otarcie w integralnym nabłonku języka.13 Następnie rozpoczyna swój cykl produkcyjny zakażając słabo zróżnicowane komórki warstw podstawnych nabłonka, gdzie rozpoczyna się transkrypcja genów.12
Gdy zainfekowane komórki różnicują się i migrują z warstwy podstawnej do warstwy kolczystej nabłonka (dopuszczalność immunologiczna), replikacja wirusowa jest stymulowana, co powoduje gromadzenie się wirionów w jądrze i tworzenie kapsydu w cytoplazmie. Istnieją co najmniej dwa cykle replikacji wirusowej: a) zakażenie lityczne i b) zakażenie lizogeniczne.
W przypadku zakażenia litycznego wirus dociera do komórek para-bazalnych ze zdolnością replikacji, przenika do cytoplazmy, a następnie do jądra. Wewnątrz jądra replikuje się w obszarze episomalnym, nie integrując się z genomem komórkowym, wytwarzając w ten sposób około 20 kopii wirusowych. Te kompletne cząstki wirusowe powodują śmierć komórki i pozostają w ten sposób wolne i w pobliżu powierzchni nabłonka.
W przypadkach infekcji lizogenicznej genom komórki jest bezpośrednio naruszony. Tak jest w przypadku wirusów HPV wysokiego ryzyka (16 i 18). Po dotarciu do jądra komórkowego wirus integruje się z genomem komórki gospodarza, głównie z segmentami E6 i E7. W tym przypadku replikacja wirusa przechodzi w fazę latencji do momentu, gdy komórka gospodarza replikuje własne DNA oraz DNA zintegrowanych wirusów. Wirusowe segmenty DNA są aktywne transkrypcyjnie po podziale komórki, co gwarantuje ich propagację.
W przeciwieństwie do zakażenia litycznego, ten typ zakażenia obserwuje się w komórkach, w których dochodzi do rozwoju złośliwego.
Wyrażenie genów różnych typów HPV jest ściśle i specyficznie regulowane przez czynniki transkrypcyjne, takie jak AP-1, czynnik specyficzny dla keratynocytów, NF-1CTF, CEFI, CEFII i TEFI oraz niektóre czynniki pochodzenia hormonalnego.
W obu typach infekcji białka E1 i E2 inicjują swoją ekspresję w kierunku wzrastającym (supraregulacja), aktywując w ten sposób transkrypcję DNA, jak również ekspresję kontrolowaną przez komórki podstawne.12
Geny E6 i E7 HPV są bezpośrednio związane z transformacją złośliwą komórek poprzez onkoproteiny E6 i E7. Białka te mają zdolność do tworzenia związków z produktami genów komórkowych regulujących cykl komórkowy, wśród których można wymienić p53 i Rb. Onkoproteina E6 tworzy związek z białkiem p53, natomiast E7 z białkiem Rb.
Białko Rb reguluje przejście z fazy G1 do S. Onkoproteina E7 sekwestruje Rb uniemożliwiając mu regulację białek proliferacji komórkowej, co zmusza cykl komórkowy do pozostawania w fazie syntezy.13 Te dwa zdarzenia: integracja genów wirusowych do genomu komórkowego oraz blokowanie prawidłowej funkcji genów supresorowych nowotworów p53 i Rb są związane z transformacją komórkową komórek zakażonych wirusami o wysokim potencjale onkogennym (16 i 18). Postępujące zmiany, których doświadczają keratocyty, modyfikują mikrośrodowisko i zmieniają równowagę nabłonka poprzez bodźce proliferacji komórkowej kierowanej wydzielaniem alfa i beta naskórkowych czynników wzrostu.
Białka E2, E3, E4, E5, E6 i E7 indukują utratę kontroli białek genowych (episomalne DNA w centrum jądra), podczas gdy E6 i E7 replikują wirusowe DNA. L1 i L2 składają wirusa i umieszczają się w dojrzałych komórkach płaskonabłonkowych, aby później ulec złuszczeniu (ponad 1000 kopii na komórkę).
W zmianach łagodnych, takich jak brodawczak języka, proliferacja cząsteczek episomalnego DNA sprzyja nieprawidłowemu wzrostowi nabłonka, zwiększając tym samym błędy genowe komórek (gastogeneza).
E6 i E7 promują proliferację wirusa i immortalizację. Gdy wirus posiada potencjał onkogenny, powoduje złośliwość, gdy nie, rozwija się zmiana łagodna, która może ulec samoograniczeniu w okresie 2 lat. Mechanizm ten indukowany jest głównie przez utratę telomerów DNA, co powoduje zahamowanie apoptozy, zwiększenie liczby zakażonych komórek oraz zmniejszenie acetylacji i fosforylacji p53 i Rb. Ponadto, dochodzi do promocji ekspresji czynników angiogennych. Tak jest w przypadku naczyniowego czynnika wzrostu, który dezorganizuje cytoszkielet komórkowy i macierz pozakomórkową wpływając na czynniki regulacyjne biorące udział w zdrowiu tych struktur.12
Zakażenie wirusemHPV powoduje istotne zmiany w morfologii komórek. Obserwuje się m.in. tworzenie wakuoli okołojądrowych, powiększenie, nieregularność i hiperchromatyczność jąder oraz dwujądrzastość. Komórki, w których doszło do tych zmian nazywane są koylocytami i uważane są za „odcisk palca” wirusa.
Kłykciny kończyste są najczęstszą manifestacją morfologiczną zakażenia HPV (condyloma acuminatum).14
PREZENTACJA PRZYPADKU
Pacjentką była 21-letnia samotna kobieta. Nie pracowała poza domem, urodziła się i mieszkała w Estado de Mexico (stan Meksyk). Jej grupa krwi to O, Rh dodatnia. W wywiadzie rodzinnym podała, że jej ojciec choruje na stwardnienie rozsiane, a siostra na reumatoidalne zapalenie stawów. Pacjentka zaprzeczyła, aby była uzależniona od narkotyków. Stwierdzono u niej liczne młodzieńcze włókniaki piersi w lewej piersi, które były leczone chirurgicznie. Menarche rozpoczęła w 15. roku życia, rytm miesiączkowania 28 × 3. Aktywność seksualną rozpoczęła w 17. roku życia. Zgłosiła jednego aktywnego seksualnie partnera, zaprzeczyła uprawianiu seksu oralnego-genitalnego. Rok wcześniej wykonano u niej badanie cytologiczne i kolposkopowe dolnych dróg rodnych oraz badanie piersi. Wyniki okazały się negatywne w kierunku raka i wirusa HPV. Metodą planowania rodziny stosowaną przez pacjentkę było urządzenie wewnątrzmaciczne.
Pacjentka po raz pierwszy zgłosiła się na konsultację w kwietniu 2014 roku, skarżąc się na glossodynię brzuszną z trzymiesięczną ewolucją. Po tym czasie doświadczyła uczucia ciała obcego i wybrzuszenia w tkance miękkiej, z postępującym wzrostem wirowym aż do uformowania guza w kształcie soczewicy, który krwawił przy kontakcie z podniebieniem twardym i podczas żucia. Zgłosiła się do gabinetu lekarskiego, gdzie otrzymała nieokreślone leczenie systemowe, które nie przyniosło zadowalających rezultatów.
Jama ustna została zbadana za pomocą procedury kolposkopii z powiększeniem 0,66x (kolposkop Hinselmann, 2014 Meksyk). Wspomniana procedura ujawniła zmianę o średnicy około 1 cm, o różowawym odcieniu, okrągłym kształcie, z poszarpanymi brzegami, bez szypuły i o charakterze awaskularnym (Rycina 1). Po zakończeniu badania pacjentka została poinformowana o rozpoznaniu i pożądanym leczeniu.
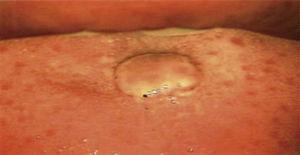
Bezpośrednie oględziny jamy ustnej w perspektywie kolposkopowej. I (Hinselmann, 2014), przy powiększeniu 0,66. Zmiana o średnicy 1cm, o różowawym odcieniu, okrągłym kształcie, poszarpanych brzegach, awaskularna i bez szypuły.
TREATMENT
W znieczuleniu miejscowym i 2% ksylokainie z epinefryną (1mL) wykonano infiltrację podstawy zmiany przy użyciu igły o kalibrze 30G. Powierzchnia zmiany została zaklipsowana i poddana ostrej dysekcji klinowej. Po uzyskaniu hemostazy, granice zmiany licowano (Dermalon 000) w jednej płaszczyźnie za pomocą szwów odwróconych. Uzyskany materiał utrwalono w 5 ml 10% formaliny i przesłano do Zakładu Patomorfologii.
Piętnaście dni później usunięto szwy i uzyskano zdrowy obszar chirurgiczny (Rycina 2). Raport histopatologiczny wykazał obecność tkanki o wymiarach 0,6 × 0,5 cm. Preparat miał nieregularny kształt, ciemnobrązowy odcień i miękką konsystencję. Analiza mikroskopowa wykazała obecność wielopostaciowego nabłonka rogówki, akantozę i hiperkeratozę. Wewnątrz próbki widoczne były różnej wielkości ogniska rogowacenia wewnątrznabłonkowego. Ogólnie, komórki nabłonka były mniejszej wielkości niż komórki prawidłowej warstwy spinosum (ryc. 3 i 4). Ostateczne rozpoznanie wskazywało na brodawczaka płaskonabłonkowego języka. Typowanie genów wirusowych przeprowadzone za pomocą reakcji łańcuchowej polimerazy (PCR) w czasie rzeczywistym wykazało obecność genotypu 58 (wirus wysokiego ryzyka).
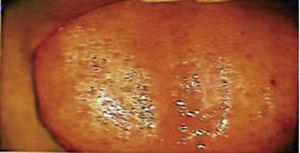
Zdjęcie języka w perspektywie kolposkopowej 15 dni po zabiegu.
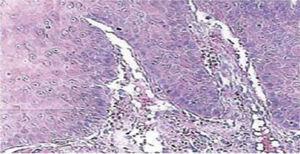
Powiększenie mikroskopowe 10x. Polistratified corneum epithelium, acanthosis and hyperkeratosis.
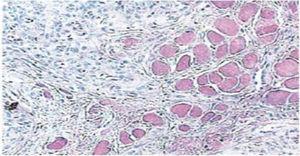
40 x Powiększenie mikroskopowe. Intra-epithelial cornification foci of different sizes.
DISCUSSION
HPV jest wirusem DNA; należy do rodziny papovaviridae, płci brodawczakowatych. Opisano ponad 230 genotypów. Okres inkubacji waha się od trzech tygodni do ośmiu miesięcy, średnio wynosi trzy miesiące. Spośród 230 genotypów brodawczaka, 16 jest najczęściej związanych ze zmianami w jamie ustnej (1, 2, 3, 4, 6, 7, 10, 11, 13, 16, 31, 32, 33, 35 i 57).
Wyróżnia się dwie główne grupy prezentacji klinicznych HPV: a) zmiany łagodne oraz b) zmiany przedzłośliwe lub złośliwe. Do łagodnych zmian w jamie ustnej zalicza się brodawczaka zwykłego, brodawczaka pospolitego, kłykciny kończyste jamy ustnej oraz ogniskową hiperplazję nabłonka (choroba Hecka). Zmiany przednowotworowe i złośliwe reprezentowane są głównie przez leukoplakię i raka kolczystokomórkowego związanego z genotypami 16 i 18. Transmisja HPV odbywa się poprzez oralno-genitalne praktyki seksualne.
Istnieje kilka technik diagnostycznych HPV, wśród których można wymienić cytologię konwencjonalną, cytologię płynnego podłoża, histologię, kolposkopię oraz techniki biologii molekularnej, takie jak hybrydyzacja in situ i łańcuchowa reakcja polimerazy (PCR).15,16 W przedstawionym przypadku klinicznym zdecydowano się na oznaczenie genotypu wirusa metodą PCR, która wykazała obecność genotypu 58. Dane te nie zostały udokumentowane w klasyfikacji podawanej w literaturze.
Leczenie jest dostosowane do każdego przypadku indywidualnie. Możliwe jest zastosowanie technik destrukcyjnych, takich jak krioterapia lub elektrochirurgia, użycie immunemodulatorów (imikwimod w stężeniu 5%), zastosowanie antymetabolitu w celu ingerencji w RNA (kwas rybo-nukleinowy) i DNA lub poprzez inhibicję syntetazy tymidylanowej (5-fluoracyl).17,18 W omawianym przypadku zdecydowano się na zabieg chirurgiczny z użyciem zimnego skalpela w oparciu o miejsce ujawnienia się zmiany, aby skorzystać z możliwości niepozostawiania następstw.
W błonie śluzowej jamy ustnej narażonej na mikrourazy, drobnoustroje oraz czynniki chemiczne i fizyczne mogą synergistycznie oddziaływać z HPV, sprzyjając rozwojowi zmian łagodnych lub raka.
HPV odgrywa istotną rolę w rozwoju raka kolczystokomórkowego w obrębie odbytu i narządów płciowych, a także w brodawkowatej epidermodysplazji i krtani.
W zmianach łagodnych najczęściej występują genotypy 33 i 32. W piśmiennictwie światowym nie opisywano genotypu 58 w tego typu zmianach, które klinicznie wydają się być łagodne.
W celu skutecznego leczenia tego schorzenia niezwykle ważna jest interdyscyplinarna diagnostyka i leczenie w gronie stomatologów, onkologów i ginekologów odpowiednio przeszkolonych w badaniu tych zmian pod kątem kolposkopowym.
Leczenie poprzez interwencję chirurgiczną z użyciem zimnego skalpela, mające na celu pozostawienie wolnych od zmian granic jest odpowiednim rozwiązaniem, aby wyeliminować ten typ zmian i nie powodować następstw, szczególnie w przypadku guzów, które wydają się być klinicznie łagodne, ale które zgodnie z ich typem genetycznym, będą ulegać złośliwemu zachowaniu w średnim i długim okresie czasu.
Uważamy, że niniejszy opis przypadku jest interesujący, ponieważ w meksykańskiej bibliografii naukowej było niewiele doniesień dotyczących tego stanu.
Wykazujemy, że jest to bardzo interesujący przypadek.